题目内容
【题目】在一个容积固定不变的密闭容器中进行反应:2A(g)+B(g) ![]() 3C(g)+D(s),已知将2mol A和1mol B充入该容器中,反应在某温度下达到平衡时,C的物质的量为W mol,C在平衡混合气体中的体积分数为n%。
3C(g)+D(s),已知将2mol A和1mol B充入该容器中,反应在某温度下达到平衡时,C的物质的量为W mol,C在平衡混合气体中的体积分数为n%。
(1)可认定上述可逆反应在一定条件下已达到化学平衡状态的是________(选填序号)。
A.体系压强不再变化 B.v正(A)=2v逆(B)
C.体系的密度不再变化 D.混合气体的平均相对分子质量不再变化
(2)如果用下列情况的配比作起始物,在同样的容器和温度下达到平衡,其结果一定是:C的物质的量为2W mol,C在平衡混合气体中的体积分数仍为n%的是___________
A. 4mol A+2mol B
B. 6mol C+1mol D
C. 1mol A+0.5mol B+1.5mol C+0.5mol D
D. 2mol A+1mol B+3mol C+1mol D
E. 2mol A+1mol B+3mol C+2mol D
(3)此反应的v—t图象如甲图,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如乙图,请用“=、<、>”填空: a1_____a2;两图中阴影部分面积:甲_____乙。
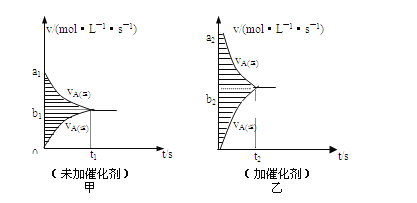
【答案】BCD ADE a1<a2 甲=乙
【解析】
(1) A.反应前后气体的物质的量总数相等,故反应过程中体系压强不变化,故压强不变不能说明到平衡,故A错误;
B.v正(A)=2v逆(B)说明正逆反应速率相等,说明到平衡,故B正确;
C.反应体系中有固体,根据质量守恒分析,当体系的密度不再变化说明气体总质量不变,即固体质量不变,说明反应到平衡,故C正确;
D.混合气体的平均相对分子质量不再变化,说明混合气体的总质量不变,反应到平衡,故D正确;
故能说明到平衡的有BCD ;
(2) A. 4mol A+2mol B 相当于原加入法的二倍,属于等效平衡,平衡时C的百分含量不变,但物质的量是原来的2倍,故A正确;
B. 6mol C+1mol D,D为固体,1mol D固体可能够达到新平衡的用量,也可能不足,不一定能满足题意,故B错误;
C.1mol A+0.5mol B+1.5mol C+0.5mol D相当于2mol A和1mol B,属于等效平衡,平衡时C的量与原来相同,故C错误;
D. 2mol A+1mol B+3mol C+1mol D相当于4mol A+2mol B,满足条件,故D正确;
E. 2mol A+1mol B+3mol C+2mol D相当于在D的基础上加了1mol D,平衡不移动,故正确;
故选 ADE;
(3).催化剂能加快反应速率,故 a1<a2;阴影部分面积表示浓度的变化量,催化剂加快反应速率,缩短到达平衡的时间,不影响平衡状态,所以到达平衡时同一物质的浓度变化量相同,故有甲=乙。

 名校课堂系列答案
名校课堂系列答案【题目】关于铝热反应的现象有如下描述:反应放出大量的热,并发出耀眼的光芒;纸漏斗的下部被烧穿,有熔融物落入沙中。已知![]() 、
、![]() 、
、![]() 、
、![]() 的熔点、沸点如表所示:
的熔点、沸点如表所示:
物质 |
|
|
|
|
熔点/℃ | 660 | 1565 | 2054 | 1535 |
沸点/℃ | 2467 | 3414 | 2980 | 2750 |
(1)某同学推测,铝热反应所得到的熔融物是铁铝合金,因为该反应放热能使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝形成铁铝合金。你认为他的解释是否合理?________(填“合理”或“不合理”)。
(2)设计一个简单的实验,证明上述熔融物中含有金属铝,填写下列表格:
①所用试剂 | ______ |
②实验操作及现象 | ______ |
③有关反应的化学方程式 | ______ |
(3)欲在常温下溶解该熔融物,下列试剂中最好选用______(填序号),理由是_________________________。
a.浓硫酸 b.稀硫酸 c.硫酸锌溶液d. ![]() 溶液
溶液