题目内容
19.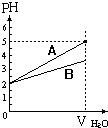 pH值等于2的两种酸溶液A和B,分别加水稀释1000倍,其pH值与所加水的体积变化趋势示意图如图所示,则下列结论正确的是:( )
pH值等于2的两种酸溶液A和B,分别加水稀释1000倍,其pH值与所加水的体积变化趋势示意图如图所示,则下列结论正确的是:( )| A. | 等体积pH=2的两种酸中和NaOH的能力酸A比酸B强 | |
| B. | A为弱酸,B为强酸 | |
| C. | 酸B的摩尔浓度比酸A大 | |
| D. | A比B易电离 |
分析 pH均为2的酸,如果酸是强酸,稀释1000倍后,溶液的pH应该为5,如果是弱酸,因为存在电离平衡,导致稀释后的溶液中氢离子大于原来的千分之一,则溶液的pH应该大于2小于5,根据图象知,溶液稀释后,A的pH为5,B的小于5,所以A是强酸,B是弱酸,据此进行判断.
解答 解:pH均为2的酸,如果酸是强酸,稀释1000倍后,溶液的pH应该为5,如果是弱酸,因为存在电离平衡,导致稀释后的溶液中氢离子大于原来的千分之一,则溶液的pH应该大于2小于5,根据图象知,溶液稀释后,A的pH为5,B的小于5,所以A为强酸、B为弱酸,
A.根据分析可知,A为强酸、B为弱酸,则B的浓度大于A,故等体积的两种酸中和强氧化钠能力B比A强,故A错误;
B.根据分析可知,A为强酸、B为弱酸,故B错误;
C.A是强酸,B是弱酸,所以B中存在电离平衡,当pH相等时,弱酸的物质的量浓度大于强酸,即:B的物质的量浓度大于A,故C正确;
D.A是强酸,B是弱酸,所以A比B容易电离,故D正确;
故选CD.
点评 本题考查强弱电解质溶液稀释时的pH的浓度变化,题目难度中等,注意明确加水稀释后促进了弱酸的电离,所以弱酸的pH变化慢,熟练掌握弱电解质的电离平衡及其影响为解答关键.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
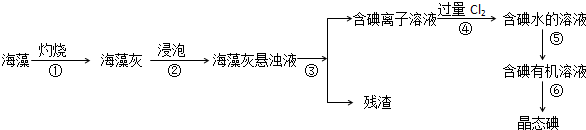
10.从海水(含氯化镁)中提取镁,涉及如下步骤:
①将沉淀物与盐酸反应,结晶、过滤 ②在HCl气体氛围中干燥产物
③过滤、洗涤沉淀物 ④将得到的产物熔融电解得到镁
⑤把贝壳制成石灰乳[Ca(OH)2],在引入的海水中加入石灰乳,沉降.
下列说法正确的是( )
①将沉淀物与盐酸反应,结晶、过滤 ②在HCl气体氛围中干燥产物
③过滤、洗涤沉淀物 ④将得到的产物熔融电解得到镁
⑤把贝壳制成石灰乳[Ca(OH)2],在引入的海水中加入石灰乳,沉降.
下列说法正确的是( )
| A. | 正确操作步骤的顺序是⑤②③①④ | |
| B. | 步骤④电解时阴极产生氯气 | |
| C. | 直接在空气中将MgCl2溶液蒸干可得到Mg(OH)2 | |
| D. | 此法提取镁的过程中涉及置换、分解、化合和复分解反应 |
7.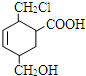 某有机物的结构简式如图所示,它在一定条件下可能发生的反应是( )
某有机物的结构简式如图所示,它在一定条件下可能发生的反应是( )
①加成反应 ②水解反应 ③酯化反应 ④氧化反应 ⑤还原反应⑥消去反应.
 某有机物的结构简式如图所示,它在一定条件下可能发生的反应是( )
某有机物的结构简式如图所示,它在一定条件下可能发生的反应是( )①加成反应 ②水解反应 ③酯化反应 ④氧化反应 ⑤还原反应⑥消去反应.
| A. | ①③④⑤⑥ | B. | ①②③④⑤ | C. | ①③⑤⑥ | D. | 全部 |
14.在25℃水中加入下列物质,不会使水的电离平衡发生移动的是( )
| A. | KI | B. | 浓氨水 | C. | 冰醋酸 | D. | 热水 |
4.下列说法或表示方法中正确的是( )
| A. | 全部由非金属元素组成的化合物中只含共价键 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 已知C(s,石墨)=C(s,金刚石)△H=+1.9 kJ/mol,则石墨比金刚石稳定 | |
| D. | 氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
11.镁条在下列那种气体中无法燃烧( )
| A. | O2 | B. | N2 | C. | Ar | D. | CO2 |
8.目前人类已发现几千万种物质,对物质进行分类,有利于我们的学习.下列关于物质的类别中,不正确的是(括号内为类别)( )
| A. | Al2O3(两性氧化物) | B. | H2SO4(含氧酸) | C. | CH3COOH(烃) | D. | 食醋(混合物) |
9.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 1molCl2与1molFe反应,转移的电子数为3NA | |
| B. | 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA | |
| C. | 在标准状况下,Cl2和H2的混合气22.4升,光照后原子总数为2NA | |
| D. | 0.1mol•L-1的FeCl3溶液中含有0.1NA个Fe3+ |