��Ŀ����
����Ŀ����ij�о���ѧϰ������H2C2O4��Һ������KMnO4��Һ֮��ķ�Ӧ��̽������������ı�Ի�ѧ��Ӧ���ʵ�Ӱ�족��ʵ�����£�
ʵ����� | ʵ���¶� | KMnO4��Һ | H2C2O4��Һ | H2O | ��Һ��ɫʱ�� | ||
V(mL) | C(mol/L) | V(mL) | C(mol/L) | V(mL) | t(s) | ||
A | 293K | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313K | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
��1��ͨ��ʵ��A��B����̽����_______�ĸı�Է�Ӧ���ʵ�Ӱ�죬����V1=_____��T1=_____��ͨ��ʵ��_______��̽�����¶ȱ仯�Ի�ѧ��Ӧ���ʵ�Ӱ�졣
��2����t1��8������ʵ��A��B���Եó��Ľ�����________________________span>������ʵ��B�����ݼ��㣬�ӷ�Ӧ��ʼ���н�������KMnO4��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ____________��
��3���÷�Ӧ������ɫ��ζ������������̱���ԭΪMn2+��д����Ӧ��Ӧ�����ӷ���ʽ_______��
��4����С���һλͬѧͨ���������Ϸ��֣���Ӧһ��ʱ���÷�Ӧ���ʻ�ӿ죬��ɴ��ֱ仯��ԭ���Ƿ�Ӧ��ϵ�е�ij�����Ӷ�KMnO4��H2C2O4֮��ķ�Ӧ��ij����������ã����������_______________����Ӧ���������п����ǣ�����ţ�_______��
II.100kPaʱ����Ӧ2NO(g)+O2(g)![]() 2NO2(g)��NO��ƽ��ת�������¶ȵĹ�ϵ������ͼ1����Ӧ2NO2(g)
2NO2(g)��NO��ƽ��ת�������¶ȵĹ�ϵ������ͼ1����Ӧ2NO2(g)![]() N2O4(g)��NO2��ƽ��ת�������¶ȵĹ�ϵ������ͼ2��
N2O4(g)��NO2��ƽ��ת�������¶ȵĹ�ϵ������ͼ2��
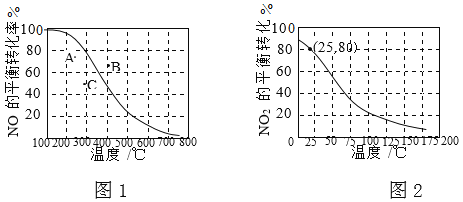
�� ͼ1��A��B��C�����ʾ��ͬ�¶ȡ�ѹǿ��2NO(g)+O2(g)![]() 2NO2(g)�ﵽƽ��ʱNO��ת���ʣ���________���Ӧ��ѹǿ���
2NO2(g)�ﵽƽ��ʱNO��ת���ʣ���________���Ӧ��ѹǿ���
�� 100kPa��25��ʱ��2NO2(g)![]() N2O4(g)ƽ����ϵ�У���ʽ����ƽ�ⳣ��Kp��________����Kp��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ���������
N2O4(g)ƽ����ϵ�У���ʽ����ƽ�ⳣ��Kp��________����Kp��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ���������
���𰸡�Ũ�� 1 293K BC ����������ͬʱ������Ӧ��Ũ�ȣ���Ӧ�������� 8.3��10��4mol/��L��s�� 2MnO42����5H2C2O4��6H��=2Mn2����10CO2����8H2O ������ Mn2�� B 0.06
��������
���ݿ��Ʊ���������Ӱ�컯ѧ��Ӧ���ʵ����������ݲ�ͬ�����¸��������Һ��ɫ�Ŀ����̶Ȳ�ͬ���ó������Ľ��ۣ���ʵ���еIJ�������������ġ�
��ij�о���ѧϰ������H2C2O4��Һ������KMnO4��Һ֮��ķ�Ӧ��̽������������ı�Ի�ѧ��Ӧ���ʵ�Ӱ������
��1��ʵ��A��B�У����������Һ��Ũ������ͬ�ģ���H2C2O4��Һ��Ũ���Dz�ͬ�ģ���ͨ��ʵ��A��B��̽����Ũ�ȵĸı�Է�Ӧ���ʵ�Ӱ�죬���ݿ��Ʊ�����ԭ����Ҫ������ʵ����¶���ͬ����Һ���������ͬ��������V1=1��T1= 293K��ͬ����B��C��ʵ����¶Ȳ�ͬ�⣬����������ͬ����ͨ��ʵ��B��C��̽�����¶ȱ仯�Ի�ѧ��Ӧ���ʵ�Ӱ�졣
��2����t1��8����ʵ��A�ĵķ�Ӧ���ʽϴ�ʵ��A�в����Ũ�ȴ���ʵ��B������ʵ��A��B���Եó��Ľ���������������ͬʱ������Ӧ��Ũ�ȣ���Ӧ������������ʵ��B�����ݼ��㣬��Ϻ���ʼŨ��c(KMnO4)=![]() ����Һ��ɫ��ʱ8s��c(KMnO4)=0������KMnO4��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ
����Һ��ɫ��ʱ8s��c(KMnO4)=0������KMnO4��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ![]() 8.3��10��4mol/��L��s����
8.3��10��4mol/��L��s����
��3���÷�Ӧ������ɫ��ζ���������������ΪCO2���̱���ԭΪMn2+���÷�Ӧ�����ӷ���ʽΪ2MnO42����5H2C2O4��6H��=2Mn2����10CO2����8H2O��
��4����С���һλͬѧͨ���������Ϸ��֣���Ӧһ��ʱ���÷�Ӧ���ʻ�ӿ죬��ɴ��ֱ仯��ԭ���Ƿ�Ӧ��ϵ�е�ij�����Ӷ�KMnO4��H2C2O4֮��ķ�Ӧ��ij����������ã����ڷ�Ӧ����һ�����¶��½��еģ��ʷ�Ӧ��ϵ�е�ij�����ӵ���������������������Ӧ�ĸ��ֲ����Ӧ���������п�����Mn2����
II.100kPaʱ����Ӧ2NO(g)+O2(g)![]() 2NO2(g)��NO��ƽ��ת�������¶ȵĹ�ϵ������ͼ1����Ӧ2NO2(g)
2NO2(g)��NO��ƽ��ת�������¶ȵĹ�ϵ������ͼ1����Ӧ2NO2(g)![]() N2O4(g)��һ��������������ٵķ�Ӧ����NO2��ƽ��ת�������¶ȵĹ�ϵ���߿�֪���¶�Խ�ߣ�NO2��ƽ��ת����ԽС����÷�ӦΪ���ȷ�Ӧ��
N2O4(g)��һ��������������ٵķ�Ӧ����NO2��ƽ��ת�������¶ȵĹ�ϵ���߿�֪���¶�Խ�ߣ�NO2��ƽ��ת����ԽС����÷�ӦΪ���ȷ�Ӧ��
������ͬ��ѹǿ�£��¶�Խ�ߣ��ﵽƽ��ʱNO��ת����ԽС����Ӧ2NO(g)+O2(g)![]() 2NO2(g)��һ��������������ٵķ��ȷ�Ӧ�����ڸ���ϵ����ƽ��ѹǿΪ100kPa�����������ϵĵ��ѹǿ����100kPa���������ϵĵ��ѹǿС��100kPa����B���Ӧ��ѹǿ���
2NO2(g)��һ��������������ٵķ��ȷ�Ӧ�����ڸ���ϵ����ƽ��ѹǿΪ100kPa�����������ϵĵ��ѹǿ����100kPa���������ϵĵ��ѹǿС��100kPa����B���Ӧ��ѹǿ���
�� 100kPa��25��ʱ��2NO2(g)![]() N2O4(g)ƽ����ϵ�У���ͼ��֪��NO2��ƽ��ת����Ϊ80%����NO2����ʼ��Ϊ1mol������仯��Ϊ0.8mol��N2O4�ı仯��Ϊ0.4mol��NO2��N2O4��ƽ�����ֱ�Ϊ0.2mol��0.4mol����ƽ����ϵ�У�NO2��N2O4����������ֱ�Ϊ
N2O4(g)ƽ����ϵ�У���ͼ��֪��NO2��ƽ��ת����Ϊ80%����NO2����ʼ��Ϊ1mol������仯��Ϊ0.8mol��N2O4�ı仯��Ϊ0.4mol��NO2��N2O4��ƽ�����ֱ�Ϊ0.2mol��0.4mol����ƽ����ϵ�У�NO2��N2O4����������ֱ�Ϊ![]() ��
��![]() ����ˣ�ƽ�ⳣ��Kp��
����ˣ�ƽ�ⳣ��Kp��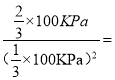 0.06��
0.06��