题目内容
9.下列关于铁电极的说法中,正确的是( )| A. | 钢铁的吸氧腐蚀中铁是正极 | |
| B. | 在铁片上镀铜时铁片作阳极 | |
| C. | 电解饱和食盐水时可用铁作阴极 | |
| D. | 镀锌铁板发生电化学腐蚀时铁是负极 |
分析 A、钢铁吸氧腐蚀氧气在正极获得电子生成氢氧根离子;
B、电镀原理中,镀件金属作阳极,镀层金属作阴极;
C、电解池中活泼金属作阳极,则阳极反应是活泼金属失电子;
D、锌铁形成原电池,锌比铁活泼作负极.
解答 解:A、钢铁吸氧腐蚀的正极发生还原反应,氧气在正极获得电子生成氢氧根离子,电极反应式为:2H2O+O2+4e-=4OH-,故A错误;
B、电镀原理中,镀件金属作阳极,镀层金属作阴极,所以铁片上镀铜时铁片作阴极,故B错误;
C、活性电极作阳极时,电极失电子,所以电解饱和食盐水时,用铁不能做阳极,可以做阴极,故C正确;
D、锌铁形成原电池,锌比铁活泼作负极,故D错误.
故选C.
点评 本题考查了原电池原理和电解池原理,题目难度不大,侧重于基础知识的考查.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.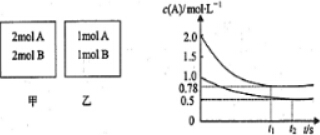 向甲乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同条件下,发生下列反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )
向甲乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同条件下,发生下列反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )
 向甲乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同条件下,发生下列反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )
向甲乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同条件下,发生下列反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )| A. | x可能等于1也可能等于2 | |
| B. | 向平衡后的乙容器中充入氮气可使c(A)增大 | |
| C. | 将乙容器单独升温可使乙容器内各物质的体积分数与甲容器内的相同 | |
| D. | 温度不变,向甲容器中再充入2mol A、2mol B,平衡时甲容器中c(A)=1.0mol•L-1 |
20.下列仪器用酒精灯加热时,需垫石棉网的是( )
①烧杯 ②坩埚 ③锥形瓶 ④蒸发皿 ⑤试管 ⑥烧瓶 ⑦表面皿.
①烧杯 ②坩埚 ③锥形瓶 ④蒸发皿 ⑤试管 ⑥烧瓶 ⑦表面皿.
| A. | ②④⑤ | B. | ①⑥⑦ | C. | ③④⑥ | D. | ①③⑥ |
17.某有机物的结构简式为HCOOCH2CH=CHCl,它不具有的官能团是( )
| A. | 酯基 | B. | 碳碳双键 | C. | 羧基 | D. | 卤原子 |
4.NA表示阿伏加德罗常数,下列说法错误的是( )
| A. | 5.6gFe与Br2完全反应,转移电子数为0.3NA | |
| B. | 常温常压下,3.2gO3所含的氧原子数为0.2NA | |
| C. | 1L 0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和小于0.1NA | |
| D. | 常温常压下,22.4LO2所含的原子数为2NA |
14.下列能说明HA是弱酸的是( )
①取0.01mol/LHA溶液测其pH大于2
②将pH等于2的HA溶液稀释100倍,pH等于4
③向pH等于4的HA溶液中加入少量NaA固体,pH变为5
④将pH等于4的HA溶液升高温度,pH基本不变
⑤HA溶液的导电性比HCI弱
⑥等pH值等体积的HA和盐酸溶液与足量的锌粒反应,盐酸放出的氢气少.
①取0.01mol/LHA溶液测其pH大于2
②将pH等于2的HA溶液稀释100倍,pH等于4
③向pH等于4的HA溶液中加入少量NaA固体,pH变为5
④将pH等于4的HA溶液升高温度,pH基本不变
⑤HA溶液的导电性比HCI弱
⑥等pH值等体积的HA和盐酸溶液与足量的锌粒反应,盐酸放出的氢气少.
| A. | ①③⑤ | B. | ②③⑥ | C. | ①③⑥ | D. | ①⑤⑥ |
18.(NH4)2S04在一定条件下发生如下反应:4(NH4)2S04=N2+6NH3+3S02+S03+7H20,将反应后的混合气体通入Ba(N03)2溶液,产生的沉淀为( )
| A. | BaS04和BaS03 | B. | BaS04 | C. | BaS03 | D. | BaS |
19.t℃时,CuSO4在水中的溶解度为25g,将32gCuSO4白色粉末加入mg水中形成饱和CuSO4溶液并有CuSO4•5H2O晶体析出,则m的取值范围是( )
| A. | 18g≤m≤128g | B. | 36g<m<180g | C. | 18g<m<128g | D. | 36g≤m≤180g |