题目内容
4.元素周期表是元素周期律的具体表现形式.下列说法正确的是( )| A. | 第二周期元素的最高正价从左向右依次从+1递增到+7价 | |
| B. | 同一周期从左到右,元素的金属性逐渐增强、非金属性逐渐减弱 | |
| C. | 第IA元素全部是金属元素 | |
| D. | 可在金属与非金属分界线附近寻找半导体材料 |
分析 A、第二周期中,O、F没有正价;
B、同一周期从左到右,元素的金属性逐渐减弱、非金属性逐渐增加;
C、IA族包含碱金属与氢元素;
D、位于金属与非金属分界线附近的元素既有金属性也有非金属性.
解答 解:A.第二周期元素中氧元素无最高正价,氟元素没有正价,故A错误;
B、同一周期从左到右,元素的金属性逐渐减弱、非金属性逐渐增加,故B错误;
C、IA族包含碱金属与氢元素,氢元素属于非金属元素,故C错误;
D、位于金属与非金属分界线附近的元素既有金属性也有非金属性,所以可在金属与非金属分界线附近寻找半导体材料,故D正确;
故选D.
点评 本题考查元素周期表的结构,比较基础,旨在考查学生对基础知识的掌握.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
15.下列有关说法正确的是( )
| A. | NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度不相同 | |
| B. | 由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀 | |
| C. | 常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| D. | 含1mol[Co(NH3)5Cl]Cl2的溶液与足量的AgNO3溶液混合,能生成2mol的AgCl沉淀 |
12.下列有关化学用语表示正确的是( )
| A. | 乙炔的结构简式:C2H2 | |
| B. | S2-的结构示意图: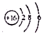 | |
| C. | 甲烷分子的球棍模型 | |
| D. | 硫酸钠的电离方程式:Na2S04=2Na++S042- |
19.在一定条件下向一密闭容器中充入2molSO2和1molO2,发生2SO2(g)+02(g)?2S03(g)的反应.下列有关说法正确的是( )
| A. | 单位时间内消耗2n molSO2的同时生成2n molS03,说明该反应达到平衡状态 | |
| B. | 达到化学平衡时,SO2、02和SO3的物质的量浓度均保持不变 | |
| C. | 达到化学平衡时,正反应和逆反应的速率都为零 | |
| D. | 达到化学平衡时,SO2将完全转化为SO3 |
9.一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )
| A. | N2、H2和NH3的质量分数不再改变 | |
| B. | c(N2):c(H2):c(NH3)=1:3:2 | |
| C. | 单位时间里每增加1molN2,同时减少2mol NH3 | |
| D. | 单位时间里每增加1molN2,同时增加3molH2 |
16.在恒容密闭容器中,通入1molH2和1molI2(g),发生反应H2(g)+I2(g)?2HI(g),在其他条件不变的情况下,改变下列条件反应速率会降低的是( )
| A. | 升高温度 | B. | 分离出HI | C. | 充入H2 | D. | 充入He |
13.下列实验设计或操作正确的是( )
| A. | 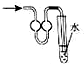 少量氨气的尾气吸收装置 | B. | 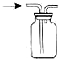 排空气法收集NO气体 | ||
| C. | 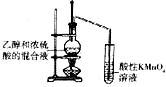 验证乙烯的生成 | D. | 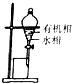 有机相从分液漏斗下口放出 |
14.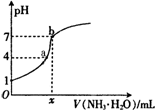 向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
 向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )| A. | x=20 | B. | 稀H2SO4的浓度为0.10mol/L | ||
| C. | b点有:2c(NH4+)=c(SO42-)>c(H+)=c(OH-) | D. | a点有:c(NH4+)<2c(SO42-) |