题目内容
【题目】Ⅰ.已知NO2和N2O4之间发生可逆反应:2NO2(g)(红棕色)![]() N2O4(g)(无色)
N2O4(g)(无色)
(1)在烧瓶A和B中盛有相同浓度的NO2与N2O4的混合气体,中间用止水夹夹紧,浸入到盛有水的烧杯中,如图所示。

分别向两个烧杯中加入浓硫酸和NH4NO3固体,观察到的现象是:A中气体红棕色加深,B中____。这说明,当条件改变时,原来的化学平衡将被破坏,并在新的条件下建立起新的平衡,即发生_____。
(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的NO2气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是______。
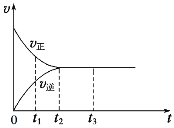
a.t1时,反应未达到平衡, NO2浓度在减小
b.t2时,反应达到平衡,反应不再进行
c.t2~t3,各物质浓度不再变化
d.t2~t3,各物质的浓度相等
e.0~t2,N2O4浓度增大
f.反应过程中气体的颜色不变
Ⅱ.某研究性学习小组欲研究影响锌和稀硫酸反应速率的外界条件,下表是其实验设计的有关数据:
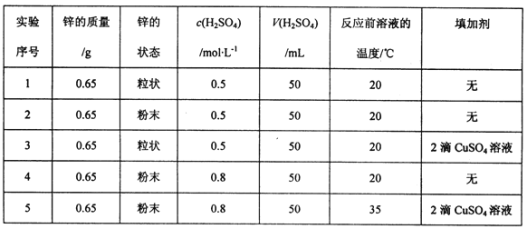
(1)在此5组实验中,判断锌和稀硫酸反应速率大小,最简单的方法可通过定量测定锌完全消失所需的时间进行判断,其速率最快的实验是_____(填实验序号)。
(2)对锌和稀硫酸反应,实验1和2表明,____对反应速率有影响。
(3)进行实验2时,小组同学根据实验过程绘制的标准状况下的气体体积V与时间t的图像如图所示。
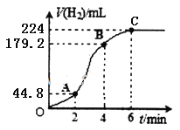
在OA、AB、BC三段中反应速率最快的是__,2~4min内以硫酸的浓度变化表示的反应速率(假设溶液的体积不变)=_____。
【答案】B中红棕色变浅 化学平衡的移动 a c e 5 固体反应物的表面积 AB 0.06mol·L-1·min-1
【解析】
Ⅰ.(1)浓硫酸的稀释是放热过程,硝酸铵的溶解过程是吸热过程,结合勒夏特列原理可知;
(2)在2NO2(g)(红棕色)![]() N2O4(g)(无色)反应中,随着反应的进行,反应物的物质的量逐渐减少,生成物的物质的量逐渐增多,当达到平衡状态时,反应物、生成物的物质的量不再改变,曲线为水平直线,以此判断题中各项;
N2O4(g)(无色)反应中,随着反应的进行,反应物的物质的量逐渐减少,生成物的物质的量逐渐增多,当达到平衡状态时,反应物、生成物的物质的量不再改变,曲线为水平直线,以此判断题中各项;
Ⅱ. (1)第5组实验时温度最高,浓度最大,也滴加了硫酸铜溶液,利用了Zn-Cu原电池;
(2)1和2除固体表面积不同外,其它因素相同;
(3)速率=浓度变化量/时间。
Ⅰ.(1)浓硫酸的稀释是放热过程,硝酸铵的溶解过程是吸热过程,所以盛有浓硫酸的烧杯中溶液温度升高、溶解硝酸铵的烧杯中溶液温度降低,A中气体颜色加深,说明正反应是放热反应,降低温度平衡正向移动,所以B中红棕色变浅。这说明,当条件改变时,原来的化学平衡将被破坏,并在新的条件下建立起新的平衡,即发生化学平衡的移动;
(2)a.t1时,反应未达到平衡,正反应速率大于逆反应速率,所以平衡正向移动,则NO2浓度在减小,故a正确;
b.t2时,正逆反应速率相等,所以反应达到平衡,反应仍然进行,为动态平衡状态,故b错误;
c.t2~t3,正逆反应速率相等,反应达到平衡状态,所以各物质浓度不再变化,故c正确;
d.t2~t3,正逆反应速率相等,反应达到平衡状态,所以各物质浓度不再变化,但各物质的浓度不相等,故d错误;
e.0~t2,正反应速率大于逆反应速率,平衡正向移动,则N2O4浓度增大,故e正确;
f.反应过程中气体的颜色变浅,达到平衡后颜色不再改变,故f错误;
答案选ace;
Ⅱ. (1)第5组实验时温度最高,浓度最大,也滴加了硫酸铜溶液,利用了Zn-Cu原电池,因此反应速率最快,锌完全消失所需的时间最短;
(2)1和2除固体表面积不同外,其它因素相同,是考查固体反应物的表面积对速率的影响;
(3)从图中看出2-4分钟内产生氢气最多,故AB这段时间内反应速率最大;
2-4分钟内,产生氢气179.2mL-44.8mL=134.4mL,物质的量为![]() =6×10-3mol,根据反应方程式:Zn+H2SO4=ZnSO4+H2↑可知,参加反应硫酸的物质的量为:6×10-3mol,v(H2SO4)
=6×10-3mol,根据反应方程式:Zn+H2SO4=ZnSO4+H2↑可知,参加反应硫酸的物质的量为:6×10-3mol,v(H2SO4)![]() =0.06molL-1min-1。
=0.06molL-1min-1。

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案【题目】已知:H2(g)+Br2(l)=2HBr(g) H=-akJ/mol,蒸发1molBr2(l)需要吸收的能量为30kJ,其他数据如下表:
H2(g) | Br2(g) | HBr(g) | |
1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | b | 369 |
下列说法正确的是
A. 2HBr(g)=H2(g)+Br2(g)H=+akJ/mol
B. H2(g)的稳定性低于HBr(g)
C. Br2(g)=Br2(l) H=+30kJ/mol
D. b=272-a


