题目内容
下列方程式中,属于水解反应的是
A.NH3 +H2O  NH3.H2O NH3.H2O |
B.HCO3— + H2O  H2CO3 + OH— H2CO3 + OH— |
C.H2O +H2O  H3O++OH— H3O++OH— |
D.HCO3— +H2O H3O+ +CO32— H3O+ +CO32— |
B
解析试题分析:A、化合反应;B、HCO3―水解,正确;C、水的自偶电离,C不正确;D、将H3O+改成H2O和H+,代入方程式消去H2O,得HCO3― H++CO32―,是电离方程式,D错;选B。
H++CO32―,是电离方程式,D错;选B。
考点 :化学用语

练习册系列答案
相关题目
关于溶液的下列说法正确的是
| A.c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能大量存在 |
| B.水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在 |
C.往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中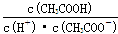 增大 增大 |
| D.等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3中c(CO32-)的大小关系为:②>④>③>① |
水的电离平衡曲线如图所示。下列说法错误的是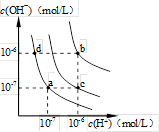
| A.水的电离常数KW数值大小关系为:b>c>d |
| B.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- |
| C.温度不变,加入少量NaOH可使溶液从c点变到 a点 |
| D.在b点对应温度下,将pH=2的HCl与pH=10的NaOH溶液等体积混合后,溶液显中性 |
弱电解质在水溶液里达到电离平衡时,溶液中已电离的电解质分子数占原总分子总数的百分数叫做该电解质的电离度。现欲粗略测定一未知浓度的醋酸溶液中醋酸的电离度,应做的实验和所需的试剂(或试纸)是
| A.电解、NaOH溶液 | B.蒸馏、Na2CO3溶液 |
| C.酯化反应、石蕊试液 | D.中和滴定、pH试纸 |
下列各溶液中,微粒的物质的量浓度关系表述正确的是
| A.0.1 mol/LNa2CO3溶液中:c(Na+)=(HCO3-)+c(H2CO3)+2c(CO32-) |
| B.常温下pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 |
| C.将0.2mol/LNaA溶液和0.1 mol·L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) |
| D.pH=l2的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 |
为比较盐酸与醋酸的酸性强弱,下列方案不可行的是(均在常温下测定)
| A.比较等体积、等pH值的两种溶液的导电性 |
| B.比较等物质的量浓度的氯化钠与醋酸钠溶液的pH值 |
| C.比较等体积、等pH值的两种溶液与过量锌粉反应产生氢气的量 |
| D.比较等体积、等物质的量浓度的两种溶液稀释相同倍数后的pH变化 |
常温下,向20.00 mL 0.1000 mol·L—1 (NH4)2SO4溶液中逐滴加入0.2000 mol·L—1NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。下列说法正确的是
| A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C.点c所示溶液中:c(SO42-)+ c(H+)= c(NH3·H2O )+ c(OH-) |
| D.点d所示溶液中:c(SO42-)>c(NH3·H2O )>c(OH-)>c(NH4+) |