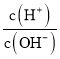题目内容
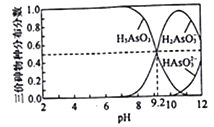
【题目】常温下,亚砷酸(H3AsO3)水溶液中含砷的各物种的分布分数(平衡时某物种的物质的量浓度占各物种的物质的量浓度之和的分数)与pH的关系如图所示。下列说祛正确的是
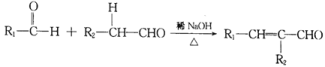
A. 以酚酞为指示剂,用NaOH溶液滴定到终点时发生的主要反应为H3AsO3+2OH-==HasO32-+H2O
B. pH=11时,溶液中有c(H2AsO3-)+2c(HAsO32-)+c(OH-)=c(H+)
C. 若将亚砷酸溶液加水稀释,则稀释过程中c(HAsO32-)/ c(H2AsO3-)减小
D. Ka1(H3AsO3)的数量级为10-10
【答案】D
【解析】根据图知,碱性条件下H3AsO3的浓度减小、H2AsO3-浓度增大,说明碱和H3AsO3生成H2AsO3-,该反应为酸碱的中和反应,同时还生成水,离子方程式为OH-+H3AsO3=H2AsO3-+H2O,A错误;pH=11时,形成NaH2AsO3和Na2HAsO3混合液,溶液中存在的电荷守恒关系为:3 c(AsO33-)+
c(H2AsO3-)+2c(HAsO32-)+c(OH-)=c(H+)+ c(Na+),B错误;
若将亚砷酸溶液加水稀释,电离平衡向右移动,由二级电离方程式可知,n(HAsO32-)增大, n(H2AsO3-)减小,则c(HAsO32-)/ c(H2AsO3-)增大,C错误;
依据图象中H3AsO3和H2AsO3-浓度相同时的PH=9.2,H3AsO3H++H2AsO3-,K a1(H3AsO3)= ![]() =c(H+)=10-9.2.mol/L,D正确。
=c(H+)=10-9.2.mol/L,D正确。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目