题目内容
【题目】(化学-物质结构与性质)氮及其化合物广泛存在于自然界中,回答下列问题:
(1)在基态15N原子的p能级上存在_____个自旋方向相同的电子;CN—中σ键与π键数目之比为_____。
(2)碱性肥料氰氨化钙(CaCN2)的组成元素中第一电离能最小的是_______(填名称)。
(3)化合物(CH3)3N能溶于水,其原因是____________________________________,(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键类型为_______________。
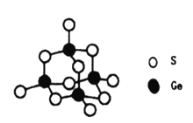
(4)阳离子[(CH3)3NH]+和阴离子A按个数比4:1组成化合物,阴离子A的结构如下图所示,则s原子的杂化轨道类型是__________,阴离子A的化学式为_______________。
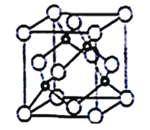
(5)立方氮化硼晶胞如下图所示(白球为氮原子,黑球为硼原子),则硼原子的配位数为___;若晶胞边长为acm,则立方氮化硼的密度是______g·cm-3(只要求列算式,阿伏加德罗常数用NA表示)。
【答案】3 1:2 钙 (CH3)3N为极性分子且能与水分子形成氢键 配位键 sp3 [Ge4S10]4- 4 100/(a3NA)
【解析】
(1)S电子云的形状为球形;N原子的电子排布式为1s22s22p3,轨道表示式为:![]() ,则p能级轨道上存在3个自旋方向相同的电子;CN-与N2为原子个数和价电子数相同的等电子体,等电子体具有相同的结构,氮气中存在氮氮三键,则CN-离子中存在碳氮三键,则离子中σ键与π键数目之比为1:2;
,则p能级轨道上存在3个自旋方向相同的电子;CN-与N2为原子个数和价电子数相同的等电子体,等电子体具有相同的结构,氮气中存在氮氮三键,则CN-离子中存在碳氮三键,则离子中σ键与π键数目之比为1:2;
(2)由于非金属性N>C>Ca,故第一电离能Ca<C<N,则第一电离能最小的是钙;
(3)(CH3)3N为结构不对称的极性分子,分子中氮原子非金属性强,原子半径小,和水之间形成氢键,所以(CH3)3N在水中溶解性增强;化合物(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键为(CH3)3N中氮原子与氢离子形成配位键;
(4)S原子的最外层电子数为6,由图可知S原子形成2个共价键,则阴离子A中S原子含有2个成键电子对和2个孤电子对,即其价层电子对数为4,属于sp3杂化;阴离子A中含有4个Ge和10个S,其中4个S只形成一个共价键,则还要得到一个电子才能形成8电子稳定结构,则A离子带有4个负电荷,即离子的化学式为[Ge4S10]4-;
(5)晶胞中N原子位于顶点和面心上,则原子数目=8×![]() +6×
+6×![]() =4,B原子位于晶胞内,则原子数目为4,故氮化硼的化学式为BN;由晶胞结构可知,B原子位于4个N原子形成的四面体的中心位置,故B原子填充N原子的正四面体空隙;晶胞的质量=
=4,B原子位于晶胞内,则原子数目为4,故氮化硼的化学式为BN;由晶胞结构可知,B原子位于4个N原子形成的四面体的中心位置,故B原子填充N原子的正四面体空隙;晶胞的质量= ![]() ,晶胞的体积为a3cm3,根据晶胞密度ρ=
,晶胞的体积为a3cm3,根据晶胞密度ρ=  。
。

 名校课堂系列答案
名校课堂系列答案【题目】锶有“金属味精”之称。以天青石(主要含有SrSO4和少量CaCO3、MgO杂质)生产氢氧化锶的工艺如下:

已知氢氧化锶在水中的溶解度:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
溶解度(g/100mL) | 0.91 | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)隔绝空气焙烧时SrSO4只被还原成SrS,化学方程式为____。
(2)“除杂”方法:将溶液升温至95℃,加NaOH溶液调节pH为12。
①95℃时水的离子积KW=1.0×10-12,Ksp[Mg(OH)2]=1.2×10-10,则溶液中c(Mg2+)=____。
②若pH过大,将导致氢氧化锶的产率降低,请解释原因____。
(3)“趁热过滤”的目的是____,“滤渣”的主要成分为___。
(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为____、过滤、洗涤、干燥。
(5)“脱硫”方法:用FeCl3溶液吸收酸浸产生的气体,吸收时的氧化产物为___(填化学式);再用石墨电极电解吸收液,电解后可在“脱硫”中循环利用的物质是__。


