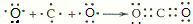��Ŀ����
6�����ֶ�����Ԫ��X��Y��Z��M��W��ԭ��������������X��Zλ��ͬ���ڣ����ǵĻ�̬ԭ���о���2��δ�ɶԵ��ӣ�Z��Wλ��ͬ���壬M�Ƕ�����Ԫ�ص�һ��������С��Ԫ�أ���1��YԪ�صĻ�̬ԭ�ӵĵ����Ų�ʽ�ǣ�1s22s22p3��
��2��X��Y��Z�γɵ�����⻯��ķе����ɸߵ��͵�˳��ΪH2O��NH3��CH4���ѧʽ����
��3��Z��һ�ֳ������⻯��˻�����ļ�����Ҫ��������������һ�ֻ�ԭ�������ĵ���ʽΪ
 ��
����4����ʵ�����У�����M2W2O8����������Һ�е�Mn 2+���������Լ�����Һ����ɫ��֤������Mn 2+���˷�Ӧ�����ӷ���ʽΪ5S2O82-+2Mn2++8H2O=10SO42-+2MnO4-+16H+��
��5����Y��Z��W��������Ԫ����ɵ�һ�����ӻ�����A����֪
��1molA��������NaOH��Һ��Ӧ���ɱ�״����22.4L���壮
��A�������ᷴӦ��������B����������ʹ��ˮ��ɫ����A��NH4HSO3���ѧʽ����A����ˮ��Ӧ�����ӷ���ʽΪHSO3-+Cl2+H2O=SO42-+2Cl-+3H+��
��6��X��s��+XO2��g��=2XO��g����Ӧ�ġ�H����ֱ�Ӳ�ã�����ͨ�������������ȼ�յķ�����Ӳ�ã���X��s����XO��g����ȼ���ȵ���ֵ�ֱ�Ϊa��b����������Ӧ�ġ�H=��2b-a��kJ/mol��
���� ������Ԫ�ػ�̬ԭ���о���2��δ�ɶԵ��ӵ���IVA���VIA�壬����X��Zֻ����̼������Yֻ���ǵ���Z��Wλ��ͬ���壬����W��������Ԫ���е�һ��������С��Ԫ�����ƣ�����M���ƣ�
��1�����ݺ��ع�����д�����Ų�ʽ���ɣ�
��2����������������۷е�ߣ�
��3��˫��ˮΪ���ۻ��������O-H����O-O�����ݴ˽�ɣ�
��4�������Լ�����Һ����ɫ��˵�������ӱ��������ɸ������������������ԭ��Ӧԭ����д���ɣ�
��5������������������ʵ�������笠��ĸ�����Ȼ������������ԭ��Ӧ�ж�S�Ĵ�����ʽΪ����������ݴ˽�ɣ�
��6����������ֱ�д��C��CO��ȼ���Ȼ�ѧ��Ӧ����ʽ��Ȼ�����ø�˹���ɽ��м��㼴�ɣ�
��� �⣺������Ԫ�ػ�̬ԭ���о���2��δ�ɶԵ��ӵ���IVA���VIA�壬����X��Zֻ����̼������Yֻ���ǵ���Z��Wλ��ͬ���壬����W��������Ԫ���е�һ��������С��Ԫ�����ƣ�����M���ƣ�
��1��Y�ǵ�Ԫ�أ�N�ĺ�����2�����Ӳ㣬ռ��3���ܼ������ݺ��ع�����д������Ų�ʽΪ��1s22s22p3���ʴ�Ϊ��1s22s22p3��
��2������O��N���γ���������۷е�ϸߣ�����ȷ˳��Ϊ��H2O��NH3��CH4���ʴ�Ϊ��H2O��NH3��CH4��
��3��˫��ˮ�Ⱦ߱������ԣ��־߱���ԭ�ԣ�˫��ˮΪ���ۻ��������O-H����O-O���������ʽΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4�������ƶϵó���M2W2O8ΪNa2S2O8����������˷�Ӧ�ķ�Ӧ��ΪNa2SO8��Mn2+��������Ϊ�����������Һ����ɫ���������ӱ��������ɸ�����������̻��ϼ�����5�ۣ���S2O82-����ԭ����SO42-������������ԭ��Ӧ���ǵ����غ�ó����ӷ�Ӧ����ʽΪ��5S2O82-+2Mn2++8H2O=10SO42-+2MnO4-+16H+��
�ʴ�Ϊ��5S2O82-+2Mn2++8H2O=10SO42-+2MnO4-+16H+��
��5��Y��Z��W��������Ԫ����ɵ�һ�����ӻ�����A����������炙�������淋ȣ���ʹ��ˮ��ɫ������Ϊ��ԭ�����壬��������ó�ӦΪ��������ӦΪ�������Σ�1molA��������NaOH��Һ��Ӧ���ɱ�״����22.4L���壬�ݴ˵ó��˻�������ֻ��1��笠����ʴ�����ӦΪNH4HSO3����������茶��л�ԭ�ԣ��������������ԣ����ݵ�ʧ�����غ��Լ�Ԫ���غ�ó����ӷ�Ӧ����ʽΪ��HSO3-+Cl2+H2O=SO42-+2Cl-+3H+���ʴ�Ϊ��NH4HSO3��HSO3-+Cl2+H2O=SO42-+2Cl-+3H+��
��6��C��s����ȼ���ȵ���ֵΪa����C��s��+O2��g��=CO2��g����H=-akJ/mol ��
CO��g����ȼ������ֵΪb����CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-bkJ/mol ��
��-�ڡ�2�ã�C��s��+CO2��g��=2CO��g�����ʡ�H=��2b-a��kJ/mol���ʴ�Ϊ����2b-a��kJ/mol��
���� ������Ԫ�ص��ƶ�Ϊ���壬�ۺϿ�����ԭ�Ӻ�������Ų�������ʽ��д���������͵��жϡ�������ԭ��Ӧ����ʽ��д���Ȼ�ѧ��Ӧ����ʽ��д���ѶȲ���

 ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д�| A�� | 58 | B�� | 29 | C�� | 14.5 | D�� | ��ȷ�� |
| A�� | 11g | B�� | 17g | C�� | 44g | D�� | 22g |
| �� ���� | ��A | ��A | ��A | ��A | ��A | ����A | ����A | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | ||
| 4 | L | M |
��2��д��CԪ�ص���̬�⻯����IԪ�ص�����������ˮ���ﷴӦ�Ļ�ѧ����ʽ��2NH3+H2SO4=��NH4��2SO4��
��3����C��D��E����Ԫ�ص��⻯�ﰴ��ԭ����ǿ��˳������ΪHF��H2O��NH3�����û�ѧʽ��ʾ��
��4��I2-��J-��L+��M2+�����У��뾶������S2-�������ӷ��ţ���
��5��A��D�γɵĻ�����A2D2�ǹ��ۻ������ۻ����ӣ��������ʽΪ
 ��
�� | A�� | 6��8 | B�� | 1��7 | C�� | 11��16 | D�� | 12��17 |
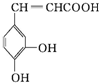
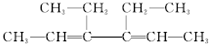
| A�� | �������б�����һ�ȴ�����2�� | |
| B�� | �÷��ӽṹ�к������ֹ����� | |
| C�� | ���ܷ���ȡ����Ӧ��Ҳ�ܷ����ӳɷ�Ӧ | |
| D�� | ����̼ԭ�Ӳ����ܶ���ͬһ��ƽ���� |
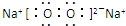 д��B���⻯��Ľṹʽ��
д��B���⻯��Ľṹʽ�� �õ���ʽ��ʾA��C��Ԫ���γ�AC2�Ĺ��̣�
�õ���ʽ��ʾA��C��Ԫ���γ�AC2�Ĺ��̣�