题目内容
【题目】某有机物含碳85.7%,含氢14.3%,向80g含溴5%的溴水中通入该有机物,溴水恰好完全褪色,此时液体总质量为81.4g.求:
(1)有机物的分子式.
(2)经测定,该有机物分子中有两个﹣CH3 , 试写出它的结构简式.
【答案】
(1)解:液体增重为81.4g﹣80g=1.4g,为有机物的质量,N(C):N(H)= ![]() :
: ![]() =7.14:14.3=1:2,该烃实验式为:CH2,为烯烃,80g含溴5%的溴水中含溴4g,物质的量为:
=7.14:14.3=1:2,该烃实验式为:CH2,为烯烃,80g含溴5%的溴水中含溴4g,物质的量为: ![]() =0.025mol,和该烃恰好反应,故该烯烃的物质的量为0.025mol,该烃的摩尔质量为:
=0.025mol,和该烃恰好反应,故该烯烃的物质的量为0.025mol,该烃的摩尔质量为: ![]() =56g/mol,
=56g/mol,
设分子式为:CnH2n,则14n=56,n=4,故分子式为:C4H8;
答:有机物的分子式案为C4H8;
(2)解:该有机物分子中有两个﹣CH3,它的结构简式可能为CH3﹣CH=CH﹣CH3、CH2=C(CH3)2,
答:它的结构简式为CH3﹣CH=CH﹣CH3、CH2=C(CH3)2
【解析】液体增重为:81.4g﹣80g=1.4g,为有机物的质量,根据碳氢质量分数可计算实验式,根据溴的量可知烃的量,计算出烃的摩尔质量结合实验式计算分子式;

【题目】甲醇合成反应及其能量变化如图a所示: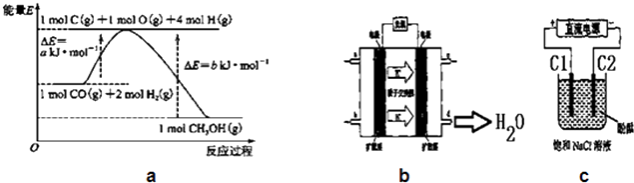
(1)写出合成甲醇的热化学方程式 .
(2)实验室在1L的密闭容器中进行模拟合成实验.将1mol CO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的浓度如下表所示:
时间浓度(mol/L)温度 | 10min | 20min | 30min | 40min | 50min | 60min |
300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
在300℃反应开始10min内,H2的平均反应速率为v(H2)= .
(3)在500℃达到平衡时,平衡常数K= .
(4)在另一体积不变的密闭容器中,充入1.2mol CO和2.0mol H2 , 一定条件下达到平衡,测得容器中压强为起始压强的一半.计算该条件下H2的转化率为 .
(5)铜基催化剂具有活性高、选择性好和条件温和的特点,已广泛地使用于CO/CO2的加氢合成甲醇.使用铜基催化剂后,该反应中a的大小变化对反应热△H有无影响, . (填“有影响”或“无影响”)
(6)2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如图b所示.请写出从C口通入O2发生的电极反应式 .
(7)用上述电池做电源,用图c装置电解饱和食盐水(C1、C2均为石墨电极).①该反应的离子方程式 .
②电解开始后在电极的周围(填“C1”或“C2”)先出现红色.

