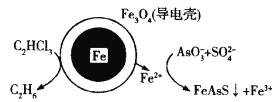
��Ŀ����
����Ŀ�����ڿ���������������ҪӦ�á�ij��ȤС����0.2 %������Һ��0.50 mol��L��1KI��0.20 mol��L��1K2S2O8��0.10 mol��L��1Na2S2O3���Լ���̽����Ӧ�����Ի�ѧ��Ӧ���ʵ�Ӱ�졣��֪��S2O82-��2I��=2SO42-��I2(��) I2��2 S2O32-=2I����S4O62-(��)
��1��Ϊ̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬��Ƶ�ʵ�鷽�����±���
ʵ����� | ���V/mL | ||||
K2S2O8��Һ | ˮ | KI��Һ | Na2S2O3��Һ | ������Һ | |
10.0 | 0.0 | 4.0 | 4.0 | 2.0 | |
9.0 | 1.0 | 4.0 | 4.0 | 2.0 | |
8.0 | V8 | 4.0 | 4.0 | 2.0 | |
��ʾV8��________mL��������__________________��
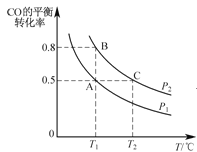
��2����֪ij�����£�Ũ��c(S2O82-)����Ӧʱ��t�ı仯������ͼ��ʾ�������������������䣬��������ͼ�У��ֱ����ͷ�Ӧ�¶Ⱥͼ������ʱc(S2O82-)��t�ı仯����ʾ��ͼ(������Ӧ�ı�ע)��_________
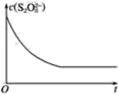
���𰸡�2.0 ������Һ�������ͬ�����ı�(S2O82-)��Ũ�ȶ���������Ũ�Ȳ��� 
��������
��1��ʵ��Ŀ����̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬�ɱ������ݿ�֪��KI��Һ��Na2S2O3��Һ������ȣ�Ӧ��̽��K2S2O8Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬������Һ�������ȣ�
��2���¶Ƚ��ͷ�Ӧ���ʼ�С��Ũ�ȱ仯��ԭ����С����Ӧ��Ҫ��ʱ�����ԭ����Ҫ��ʱ�䣬ʹ�ô�������Ӧ���ʼӿ죬Ũ�Ȳ��䣬�Դ˻���c(S2O82-)��t�ı仯����ʾ��ͼ��
(1)ʵ��Ŀ����̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬�ɱ������ݿ�֪��KI��Һ��Na2S2O3��Һ������ȣ�Ӧ��̽��K2S2O8Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬������Һ�������ȣ��������������䣬ֻ�ı䷴Ӧ��K2S2O8Ũ�ȣ��Ӷ��Ŵﵽ����ʵ��Ŀ�ģ���Vx=10.0mL8.0mL=2.0mL��
�ʴ�Ϊ��2.0����֤��Һ���������,�������������䣬ֻ�ı䷴Ӧ��K2S2O8Ũ�ȣ��Ӷ��Ŵﵽ����ʵ��Ŀ�ģ�
��2���¶Ƚ��ͷ�Ӧ���ʼ�С��Ũ�ȱ仯��ԭ����С����Ӧ��Ҫ��ʱ�����ԭ����Ҫ��ʱ�䣬ʹ�ô�������Ӧ���ʼӿ죬Ũ�Ȳ��䣬�Դ˻���c��S2O82-����t�ı仯����ʾ��ͼΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��

 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д� �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д�