题目内容
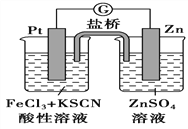
【题目】如图为原电池装置示意图。
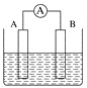
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是_____(填字母)。
A.铝片、铜片 B.铜片、铝片
C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式____
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O。写出B电极反应式___,该电池在工作时,A电极的质量将___(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为___。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:_____;该电池在工作一段时间后,溶液的碱性将_____(填“增强”“减弱”或“不变”)。
【答案】B Al-3e-+4OH-===![]() +2H2O PbO2+
+2H2O PbO2+![]() +4H++2e-===PbSO4+2H2O 增加 0.1NA H2+2OH--2e-===2H2O 减弱
+4H++2e-===PbSO4+2H2O 增加 0.1NA H2+2OH--2e-===2H2O 减弱
【解析】
(1)铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,根据负极金属单质上电子来判断;碱性条件下,Al失电子生成偏铝酸根离子;
(2)B为PbO2,是原电池的正极,发生还原反应,注意电解质溶液是硫酸;A是Pb,其离子能够与硫酸根反应生成沉淀;据电池反应式计算;
(3)氢氧燃料电池中,氢气在负极发生氧化反应,碱性环境中生成水,氢氧燃料电池反应生成水,导致电解质溶液浓度降低。
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,铝钝化,所以Cu失电子作负极,一组插入烧碱溶液中,Cu与氢氧化钠不反应,Al失电子作负极,碱性条件下,Al失电子生成偏铝酸根离子,其电极反应为:Al+4OH--3e-=AlO2-+2H2O;
(2)B为PbO2,是原电池的正极,发生还原反应,电解质溶液是硫酸,铅离子能够与硫酸根离子生成沉淀,电极反应式为:PbO2+SO42-+4H++2e-=PbSO4+2H2O;A极Pb失电子生成铅离子能够与硫酸根反应生成沉淀,导致质量增大;据电池反应式可知,每有2mol硫酸反应转移电子2mol,则0.1mol硫酸反应转移电子数目为0.1NA;
(3)氢氧燃料电池中,氢气在负极发生氧化反应,碱性环境中生成水,A为负极,负极的电极反应式为:H2+2OH--2e-=2H2O,因为生成水,导致电解质溶液的浓度减小,所以KOH溶液的碱性减弱。

 名校课堂系列答案
名校课堂系列答案