题目内容
2.放射性同位素钬${\;}_{67}^{166}$Ho的原子核内的中子数与核外的电子数之差是( )| A. | 32 | B. | 67 | C. | 99 | D. | 166 |
分析 67166Ho中质子数为67,质量数为166,中子数=质量数-质子数,核外电子数=核电荷数,据此分析解答.
解答 解:67166Ho中质子数为67,质量数为166,中子数=质量数-质子数=166-67=99,由题意知核外电子数等于核电荷数为67,该同位素原子核内的中子数与核外电子数之差为:99-67=32.
故选A.
点评 本题考查质子数、中子数、核外电子数及其相互联系,题目难度不大,明确在原子中:质子数=电子数=核电荷数;质量数=质子数+中子数是解题的关键.

练习册系列答案
 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
13.25℃时,H2SO3?HSO${\;}_{3}^{-}$+H+的电离平衡常数Kh=1×10-2,下列说法不正确的是( )
| A. | 该温度下NaHSO3 的水解平衡常数Kh=1×10-2 | |
| B. | 若向NaHSO3 溶液中加入少量的I2,则溶液中$\frac{c{(H}_{2}{SO}_{3})}{c(HS{O}_{3}^{-})}$ 将减小 | |
| C. | 略微升高温度 Ka(H2SO3)和 Kh(NaHSO3)均增大 | |
| D. | NaHSO3溶液中:c(H+)<c(S${O}_{3}^{2-}$)+c(HSO${\;}_{3}^{-}$)+c(OH-) |
17.对下列事实的解释不正确的是( )
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 反应CuSO4+H2S=CuS↓+H2SO4,说明硫化铜既不溶于水,也不溶于稀硫酸 | |
| C. | 常温下浓硫酸、浓硝酸可以用铝罐储存,说明浓硫酸、浓硝酸与铝不反应 | |
| D. | 漂白粉长期放置在空气中会失效,说明其主要成分与空气中的某成分发生了反应 |
7.下列物质中,只含有离子键的是( )
| A. | NaOH | B. | NH4Cl | C. | MgCl2 | D. | H2O |
14.下列有关电能特点的说法错误的是( )
| A. | 电能是现代社会应用最广泛,使用最方便,污染最小的二次能源 | |
| B. | 目前我国发电总量中火电所占比率最多 | |
| C. | 燃煤发电过程中能量转换方式为:化学能→热能→机械能→电能 | |
| D. | 火力发电过程中能量转化率很高 |
11.下列有机反应属于加成反应的是( )
| A. | CH2=CH-CH3+Cl2$\stackrel{高温}{→}$CH2=CHCH2Cl+HCl | |
| B. | 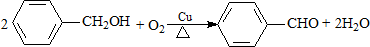 | |
| C. | 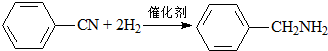 | |
| D. | 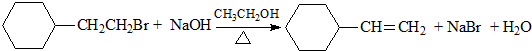 |
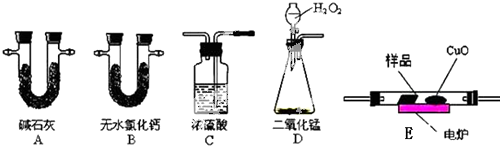
 取4.4g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重8.8g,B管增重3.6g.请回答:
取4.4g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重8.8g,B管增重3.6g.请回答: