题目内容
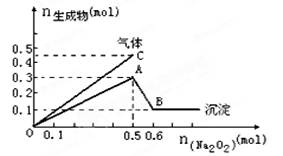
向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中三种离子的物质的量之比为

| A.2∶1∶2 | B.1∶2∶2 | C.2∶2∶1 | D.9∶2∶4 |
A
2Na2O2+2H2O=4NaOH+O2↑ NH4++OH-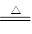 NH3↑+H2O
NH3↑+H2O
可知,加入的0.5 molNa2O2会产生0.25mol的氧气,而图中共产生0.45mol的气体,所以同时有0.2mol的氨气生成,进而可知原溶液中的NH4+为0.2mol;
图示中由A点到B点,沉淀的物质的量由0.3mol降至0.1mol,可知其中有0.1mol的Mg(OH)2,有0.2mol的Al(OH)3,依据原子守恒可知,原溶液中的Mg2+、Al3+物质的量分别为0.1mol、0.2mol,故原溶液中三种离子的物质的量之比为2∶1∶2,答案为A
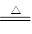 NH3↑+H2O
NH3↑+H2O可知,加入的0.5 molNa2O2会产生0.25mol的氧气,而图中共产生0.45mol的气体,所以同时有0.2mol的氨气生成,进而可知原溶液中的NH4+为0.2mol;
图示中由A点到B点,沉淀的物质的量由0.3mol降至0.1mol,可知其中有0.1mol的Mg(OH)2,有0.2mol的Al(OH)3,依据原子守恒可知,原溶液中的Mg2+、Al3+物质的量分别为0.1mol、0.2mol,故原溶液中三种离子的物质的量之比为2∶1∶2,答案为A

练习册系列答案
相关题目
 子的浓度如下表,则M离子可能为:
子的浓度如下表,则M离子可能为: )与加入NaOH溶液的体积(
)与加入NaOH溶液的体积(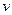 )的关系如右图所示。
)的关系如右图所示。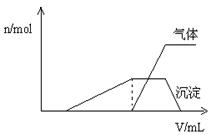
 __ ___ __;
__ ___ __; Cl- 、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积标准状况)的关系如下表所示,分析后回答下列问题:
Cl- 、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积标准状况)的关系如下表所示,分析后回答下列问题: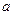 mol
mol