题目内容
【题目】某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
I.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g 苯甲酸和20 mL 甲醇(密度约0.79g · mL-1) ,再小心加入3 mL 浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是_________;若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:__________________。
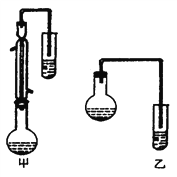
(2)甲和乙两位同学分别设计了如上图两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用_________装置(填“甲”或“乙”)。理由是___________________。
(3)反应物CH3 OH 应过量,理由是__________________________________。
II.粗产品的精制
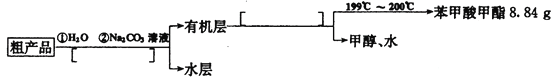
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现按下列流程图进行精制,请在流程图中方括号内填入恰当操作方法的名称______________。
(5)通过计算,苯甲酸甲酯的产率为_________________________。
【答案】 催化剂、吸水剂 ![]() 甲 甲采用冷凝回流装置,减少了CH3OH 的挥发,产率高(或由于苯甲酸和苯甲酸甲酯的沸点远高于甲醇,蒸出酯的温度在200 ℃ 左右,此时甲醇会大量蒸发,不利于合成反应,所以应冷凝回流) 该反应是可逆反应,增加CH3OH 的量,使平衡向右移动,有利于提高苯甲酸的转化率 分液 蒸馏 65 %
甲 甲采用冷凝回流装置,减少了CH3OH 的挥发,产率高(或由于苯甲酸和苯甲酸甲酯的沸点远高于甲醇,蒸出酯的温度在200 ℃ 左右,此时甲醇会大量蒸发,不利于合成反应,所以应冷凝回流) 该反应是可逆反应,增加CH3OH 的量,使平衡向右移动,有利于提高苯甲酸的转化率 分液 蒸馏 65 %
【解析】I.(1) 酯化反应为可逆反应,反应中浓硫酸起到催化剂的作用,且浓硫酸具有吸水性,有利于平衡正向移动,所以浓硫酸的作用是催化剂、吸水剂;酯化反应规律:羧酸脱羟基,醇脱羟基中的氢,因此反应产物水分子中有同位素18O,那么18O一定存在羧酸中的羟基氧上,化学方程式为:![]() ;正确答案:催化剂、吸水剂;
;正确答案:催化剂、吸水剂;![]() 。
。
(2)由装置图可以知道,甲图的圆底烧瓶上有冷凝管,起到冷凝回流作用,乙图则没有,而本题中反应物甲醇沸点低,苯甲酸、苯甲酸甲酯的沸点远高于甲醇,若采用乙图,甲醇必定会大量挥发,不利于合成反应,所以应冷凝回流,减少甲醇的挥发,提高产率;正确答案:甲;甲采用冷凝回流装置,减少了CH3OH 的挥发,产率高(或由于苯甲酸和苯甲酸甲酯的沸点远高于甲醇,蒸出酯的温度在200 ℃ 左右,此时甲醇会大量蒸发,不利于合成反应,所以应冷凝回流)。
(3)酯化反应为可逆反应,增加CH3OH 的量,使平衡向右移动,有利于提高苯甲酸的转化率;正确答案:该反应是可逆反应,增加CH3OH 的量,使平衡向右移动,有利于提高苯甲酸的转化率。
II.(4)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,先加入水可以溶解硫酸,再加入饱和的Na2CO3溶液,既可以反应消耗苯甲酸,也可以降低苯甲酸甲酯的溶解度。由于它们是互不相溶的液体,因此可常用分液的方法分离;在分液得到的有机物中因为甲醇与苯甲酸甲酯的沸点不同,将它们通过蒸馏分离开来;正确答案:分液、 蒸馏。
(5)已知苯甲酸的质量为12.2g,其物质的量为0.1mol;甲醇的质量为15.8g,其物质的量为0.49mol;根据化学方程式:![]() 可知,按苯甲酸进行计算,理论上应制得苯甲酸甲酯13.6g,所以苯甲酸甲酯的产率为8.84/13.6×100%=65%;正确答案:65 %。
可知,按苯甲酸进行计算,理论上应制得苯甲酸甲酯13.6g,所以苯甲酸甲酯的产率为8.84/13.6×100%=65%;正确答案:65 %。