题目内容
按要求填空.
(1)写出下列物质或微粒的电子式
①KOH ;②Ar ;③N2;④镁离子 ;⑤硫离子 ;⑥H2;
(2)写出下列物质的结构式
①CH4;②H2O ; ③Cl2.
(1)写出下列物质或微粒的电子式
①KOH
(2)写出下列物质的结构式
①CH4;②H2O
考点:电子式,结构式
专题:化学键与晶体结构
分析:(1)简单阳离子的电子式为其离子符合,复杂的阳离子电子式除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号的右上方标出离子所带的电荷.无论是简单阴离子,还是复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电荷. 离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后.)拼在一起.对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写;以共价键形成的物质,必须正确地表示出共用电子对数,并满足每个原子的稳定结构,共价化合物电子式的书写,一般为正价者在前.对于不同价态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边;
(2)将电子式中的共用电子对换成短线,即为化合物的结构式,根据各物质的电子式写出其结构式.
(2)将电子式中的共用电子对换成短线,即为化合物的结构式,根据各物质的电子式写出其结构式.
解答:
解:(1)①KOH:氢氧化钾为离子化合物,氢氧根离子需要标出最外层电子,氢氧化钾的电子式为: ,
,
故答案为: ;
;
②Ar 为稀有气体的原子,最外层为8个电子,其电子式为: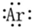 ,
,
故答案为: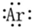 ;
;
③N2:氮气分子中存在1个氮氮三键,氮气的电子式为: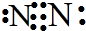 ,
,
故答案为: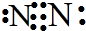 ;
;
④镁离子为简单阳离子,直接用离子符号表示其电子式:Mg2+,
故答案为:Mg2+;
⑤硫离子为阴离子,电子式中需要标出所带电荷及最外层电子,硫离子的电子式为: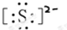 ,
,
故答案为: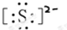 ;
;
⑥H2:氢气分子中存在1个H-H共用电子对,氢气的电子式为H:H,
故答案为:H:H;
(2)①CH4:甲烷为正四面体结构,分子中存在4个碳氢键,甲烷的电子式为: ,则甲烷的结构式为:
,则甲烷的结构式为: ,
,
故答案为: ;
;
②H2O:水分子中存在2个氧氢键,水的电子式为: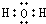 ,则水的结构式为:H-O-H,
,则水的结构式为:H-O-H,
故答案为:H-O-H;
③Cl2:氯气分子中存在1个Cl-Cl共价键,氯气的电子式为: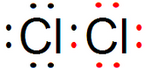 ,则氯气的结构式为:Cl-Cl,
,则氯气的结构式为:Cl-Cl,
故答案为:Cl-Cl.
 ,
,故答案为:
 ;
;②Ar 为稀有气体的原子,最外层为8个电子,其电子式为:
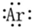 ,
,故答案为:
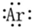 ;
;③N2:氮气分子中存在1个氮氮三键,氮气的电子式为:
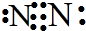 ,
,故答案为:
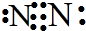 ;
;④镁离子为简单阳离子,直接用离子符号表示其电子式:Mg2+,
故答案为:Mg2+;
⑤硫离子为阴离子,电子式中需要标出所带电荷及最外层电子,硫离子的电子式为:
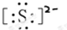 ,
,故答案为:
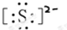 ;
;⑥H2:氢气分子中存在1个H-H共用电子对,氢气的电子式为H:H,
故答案为:H:H;
(2)①CH4:甲烷为正四面体结构,分子中存在4个碳氢键,甲烷的电子式为:
 ,则甲烷的结构式为:
,则甲烷的结构式为: ,
,故答案为:
 ;
;②H2O:水分子中存在2个氧氢键,水的电子式为:
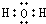 ,则水的结构式为:H-O-H,
,则水的结构式为:H-O-H,故答案为:H-O-H;
③Cl2:氯气分子中存在1个Cl-Cl共价键,氯气的电子式为:
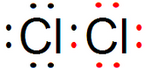 ,则氯气的结构式为:Cl-Cl,
,则氯气的结构式为:Cl-Cl,故答案为:Cl-Cl.
点评:本题考查了电子式、结构式的书写,题目难度中等,试题涉及的题量较大,注意掌握电子式、结构式的概念及正确的书写方法,明确原子、阴阳离子的电子式的区别.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度(mol/L) | 0.1 | 0.2 | 0 |
| 平衡浓度(mol/L) | 0.05 | 0.15 | 0.1 |
| A、反应达到平衡时,X的转化率为50% | ||
B、反应可表示为X+Y?2Z,其平衡常数为
| ||
| C、若该反应为放热反应,升高温度,平衡常数减小 | ||
| D、增大压强使平衡向生成Z的方向移动,平衡常数不变 |
下列液体混合物中,可用分液漏斗分离的一组是( )
| A、溴和四氯化碳 |
| B、苯和溴苯 |
| C、乙醇和乙酸 |
| D、硝基苯和水 |
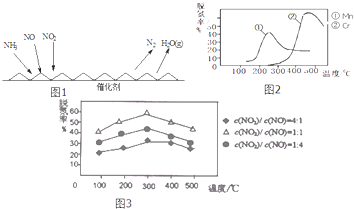

 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.