题目内容
20.下列不能证明反应N2(g)+3H2(g)?2NH3(g)已达到化学反应的限度的是( )| A. | v正(NH3)=3v逆(H2) | |
| B. | 1个N≡N键断裂的同时有6个N-H键断裂 | |
| C. | 反应体系压强不再变化 | |
| D. | 混合气体质量不再变化 |
分析 根据化学反应到达平衡时,正逆反应速率相等,各物质的物质的量浓度不再发生变化来进行判断.
解答 解:A、反应速率之比等于化学计量数之比,所以当3v正(NH3)=2v逆(H2)时,反应达到平衡状态,A中没有达到平衡状态,故A选;
B、2mol氨气分子有6molN-H键1个N≡N键断裂的同时有6个N-H键断裂,说明正逆反应速率相等,反应达到平衡状态,故B不选;
C、该反应中前后气体的物质的量不等,压强不变达到平衡状态,故C不选;
D、据质量守恒定律,混合气体的质量始终不变,所以,混合气体的质量不变不能说明反应达到平衡状态,故D选;
故选AD.
点评 本题考查平衡状态的判断,对于反应前后气体的计量数之和不相等的可逆反应来说,可从浓度、压强、百分含量等角度判断是否达到平衡状态.

练习册系列答案
相关题目
11.下列反应中原子利用率高,符合“绿色化学”要求,无污染环境因素的是( )
| A. | 乙烷与Cl2反应制氯乙烷 | B. | 乙醇和浓硫酸共热制乙烯 | ||
| C. | 乙酸和乙醇共热酯化 | D. | 乙烯与氧气在银催化作用下生成 |
8.下列各组物质最简式相同,但既不是同系物,又不是同分异构体的是( )
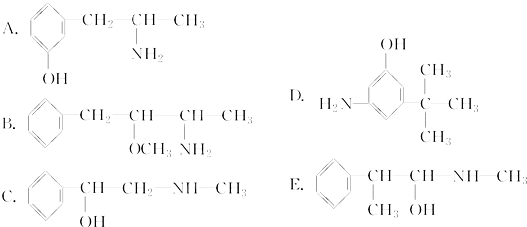
| A. | CH3CH═CH2和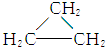 | B. | 乙炔和苯 | C. | 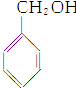 和 和 | D. | 乙酸和甲酸甲酯 |
5.下列变化过程,属于放热过程的是( )
①液态水变成水蒸气; ②酸碱中和反应; ③浓H2SO4稀释;
④固体氢氧化钠溶于水; ⑤H2在Cl2中燃烧; ⑥碳与水蒸气生产水煤气;
⑦NH4Cl晶体与Ba(OH )2•8H2O混合搅拌.
①液态水变成水蒸气; ②酸碱中和反应; ③浓H2SO4稀释;
④固体氢氧化钠溶于水; ⑤H2在Cl2中燃烧; ⑥碳与水蒸气生产水煤气;
⑦NH4Cl晶体与Ba(OH )2•8H2O混合搅拌.
| A. | ①③⑤ | B. | ①⑥⑦ | C. | ②④⑦ | D. | ②③④⑤ |
12.绿色能源是指使用不会对环境造成污染的能源.下列属于绿色能源的是( )
①太阳能 ②风能 ③潮汐能 ④煤 ⑤天然气 ⑥石油.
①太阳能 ②风能 ③潮汐能 ④煤 ⑤天然气 ⑥石油.
| A. | ①②③ | B. | ③④ | C. | ④ | D. | ①②⑥ |
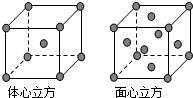 A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P轨道中有3个未成对电子,D元素原子核外的M层中只有2对成对电子.
A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P轨道中有3个未成对电子,D元素原子核外的M层中只有2对成对电子.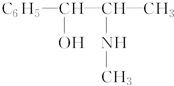
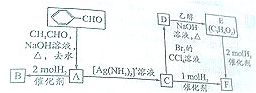
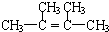 ;
;
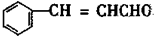 B
B C
C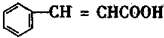 D
D
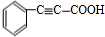 +2H2$→_{△}^{催化剂}$
+2H2$→_{△}^{催化剂}$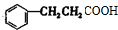 ;加成反应;.
;加成反应;.