��Ŀ����
����Ŀ���±���ʵ����Ԫ�����ڱ��IJ��ֱ߽磬�����ϱ߽粢δ��ʵ�߱����

������Ϣ�ش��������⡣
��1�����ڱ��л�̬Gaԭ�ӵ����������Ų�ʽΪ ��
��2��FeԪ��λ�����ڱ��� ����Fe��CO���γ������Fe(CO)5����Fe(CO)5�����Ļ��ϼ�Ϊ ����֪��ԭ����Ŀ�͵�������(��۵�������)��ͬ������Ϊ�ȵ����壬�ȵ�����������ƵĽṹ��������CO���ӻ�Ϊ�ȵ�����ķ��Ӻ����ӷֱ�Ϊ �� (�ѧʽ)��
��3����CH4��CO2��CH3OH�У�̼ԭ�Ӳ�ȡsp3�ӻ��ķ����� ��
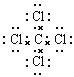
��4������VSEPR����Ԥ��ED4-���ӵĿռ乹��Ϊ ��B��C��D��Eԭ��������γɵķ����У�����ԭ�Ӷ����������8�����ȶ��ṹ�ķ��ӵĵ���ʽΪ (д2��)��
���𰸡���1��4s24p1��2��d 0 N2CN����3��CH4��CH3OH ��4���������� CO2��NCl3��CCl4(��д2�ּ���)
�������������������1��31��Ԫ��Gaԭ�ӻ�̬�����������Ų�ʽΪ4s24p1����2��26��Ԫ��FeԪ�������ڱ���λ�ڵ������ڵ����壬λ�����ڱ���d����Fe��CO���γ������Fe(CO)5����Fe(CO)5�����Ļ��ϼ�Ϊ0�ۡ���CO���ӻ�Ϊ�ȵ�����ķ�����N2������ΪCN������3����CH4��CO2��CH3OH�У�̼ԭ�Ӳ�ȡsp3�ӻ��ķ�����CH4��CH3OH��CO2�е�Cԭ�ӵ��ӻ���ʽΪsp�ӻ�����4�����ݱ����и���Ԫ�ص����λ�ÿ��Կ�����A��H��B��C��C��N��D��O��E��Cl������VSEPR����Ԥ��ClO4-���ӵĿռ乹��Ϊ���������͡���C��N��O��Clԭ��������γɵķ����У�����ԭ�Ӷ����������8�����ȶ��ṹ�ķ�����CO2��NCl3��CCl4�������ʽΪ![]() ��
��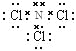 ��
�� ��
��

����Ŀ��һ�����ø������̻�(��Fe��Mn��SiO2��������Al2O3��CaO��MgO)�Ʊ�MnCO3�Ĺ����������£�
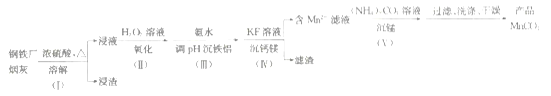
��֪25��ʱ��������������ܶȻ�������
������ | CaF2 | MgF2 | MnCO3 | Mn(OH)2 |
Ksp | 4.0��10-11 | 6.4��10-9 | 2.2��10-11 | 1.9��10-13 |
�ش��������⣺
(1)����(��)��������Ҫ�ɷ���______________(�ѧʽ)��
(2)����(��)��H2O2��Һʱ��Ӧ�����ӷ���ʽΪ________________��
�Ӱ�ˮ����pH������ʱ������(��)Ӧ���ڵ�pH���˷�ΧΪ____________��(���ֽ������ӿ�ʼ�����������ȫ��pH��Χ����)
�������� | Fe2+ | Fe3+ | Al3+ | Mn2+ | Mg2+ |
����pH��Χ | 7.6��9.6 | 2.7~3.7 | 3.4~5.2 | 8.3~9.3 | 9.6��11.1 |
(3)����(��)��KF��Һ����þʱ��Ҫʹc(Ca2+)��c(Mg2+)��С��1��10-6mol��L-1����Ӧ���Ʒ�ӦҺ��c(F-)>___________mol��L-1����ӦMgF2(s)+Ca2+![]() CaF2(s)+Mg2+��ƽ�ⳣ��K=___________��
CaF2(s)+Mg2+��ƽ�ⳣ��K=___________��
(4)���������ʱ����60�水Ͷ�ϱ�n[(NH4)2CO3]/n(Mn2+)=2����Һ��pH��MnCO3���ʵ�Ӱ����ͼ��ʾ��pH=7����Ͷ�ϱ�n[(NH4)2CO3]/n(Mn2+)=2����Ӧ�¶ȶ�MnCO3���ʵ�Ӱ����ͼ��ʾ��
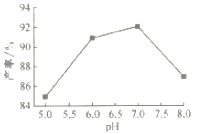
����ͼ�У���pH<7.0ʱ��pHԽС����____________(����Խ��������Խ��������pH>7.0ʱ��pHԽ�����Խ���Ҵ���Ҳ���ͣ���ԭ����___________________��

����ͼ�У��¶ȸ���60��ʱ���¶�Խ�߲���Խ���Ҵ���ҲԽ�ͣ���Ҫԭ����______________��



