题目内容
5.在含有Fe2+、Fe3+、Al3+、NH4+的溶液中加入足量的Na2O2固体,再加入过量的稀HCl,完全反应后,离子数目几乎没有改变的是( )| A. | Fe2+ | B. | Fe3+ | C. | Al3+ | D. | NH4+ |
分析 Na2O2可与水反应生成NaOH,且具有强氧化性,具有还原性的离子或与OH-反应的离子不能大量共存,再通入过量氯化氢,可与碱、偏铝酸钠等反应,以此来解答.
解答 解:加入足量过氧化钠,过氧化钠具有强氧化性且和水反应生成NaOH,Fe2+被氧化生成Fe3+,Al3+→AlO2-,Fe3+→Fe(OH)3,NH4+变成氨气放出,加入盐酸后,AlO2-和Fe(OH)3分别又生成Al3+、Fe3+,则溶液中Fe3+增多,Fe2+、NH4+减小,Al3+不变,
故选C.
点评 本题考查离子反应及离子共存,为高频考点,把握过氧化钠性质及整个过程中发生的反应是解本题关键,注意过氧化钠的强氧化性,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.糖原[(C6H10O5)n]是一种相对分子质量比淀粉更大的多糖.主要存在于肝脏和肌肉中,常常称为动物淀粉或肝糖.下列有关糖原的叙述中正确的是( )
| A. | 糖原与纤维素互为同分异构体,与淀粉互为同系物 | |
| B. | 糖原能溶于水,有甜味 | |
| C. | 糖原水解的最终产物是葡萄糖 | |
| D. | 糖原具有还原性,是还原性糖 |
16.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间的转化关系如下图所示.下列有关物质的推断正确的是 ( )
( )
 ( )
( )| 甲 | 乙 | 丙 | 丁 | |
| A | S | SO2 | SO3 | O2 |
| B | CO32- | HCO3- | CO2 | H+ |
| C | Cl2 | FeCl3 | FeCl2 | Fe |
| D | Al3+ | Al(OH)3 | AlO2- | NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
13.下列有关化学用语使用正确的是( )
| A. | CO2的电子式: | |
| B. | 具有16个质子、16个中子和18个电子的微粒是${\;}_{16}^{32}$S | |
| C. | 甲酸钠的分子式:CHO2Na | |
| D. | 乙烯的比例模型: |
17.某研究性学习小组设计了用化学电源使LED灯发光的装置,示意图如图.下列说法不正确的是( )

| A. | 锌是负极,电子从锌片经导线流向铜片 | |
| B. | 氢离子在铜片表面被还原 | |
| C. | 锌质量减少65g时,铜电极表面析出氢气是22.4L | |
| D. | 装置中存在“化学能→电能→光能”的转换 |

 +2
+2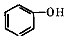 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +H2O
+H2O +SOCl2→
+SOCl2→ +SO2+HCl
+SO2+HCl +HCl
+HCl .
.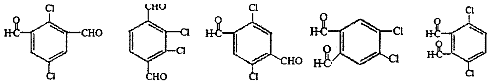 (其中两种).
(其中两种).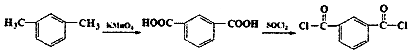 .
.