��Ŀ����
8����������п��M=455g•mol-1���ǽ�����������һ�ֲ�пʳƷ���Ӽ�����������пΪ��ɫ�ᾧ�Է�ĩ��������ˮ����������ˮ����������ˮ�Ҵ����ȷº����ѣ�140��-150�濪ʼ�ֽ⣮�ɲ���ֱ�Ӻϳɷ����䷴Ӧ��Ca��C6H11O7��2����������ƣ�+ZnSO4�TZn��C6H11O7��2����������п��+CaSO4����ʵ������Ϊ��
�Իش��������⣺
��1���Ʊ���������пʱ���ɷ����Ȼ�п��������п����ԭ��Ϊ�Ȼ���������ˮ�������ϸ��ֽⷴӦ��������
��2���ڡ���Ӧ��ʱ�����90�棬���Բ��ü��ȷ�ʽΪˮԡ���ȣ���Ӧ������90���ԭ��Ϊ��Ӧ���¶ȹ��ͣ���Ӧ���������¶ȹ��ߣ�������п���ֽ⣮
��3���ڡ���ȴ��Һ��ʱ����95%�Ҵ���Ŀ��Ϊ����������п���ܽ�ȣ�����������
��4���ֲ�Ʒ���ᴿ����Ϊ�ؽᾧ��ѡ����Լ�������˳����ȷ����D
A.95%�Ҵ�����ˮ
B����ˮ��95%�Ҵ�
C.95%�Ҵ���90����ˮ��
D.90����ˮ��95%�Ҵ�
��5���ᴿ��IJ�Ʒ�����Ը���T��BET��Ϊָʾ������EDTA���вⶨ����ԭ�����£�
Zn2+��RET�����γɾƺ�ɫ��Zn-RET������EDTA��Zn2+���������ǿ���ʷ����·�Ӧ��Zn-RET���ƺ�ɫ��+EDTA����ɫ���TZn-EDTA����ɫ��+BET������ɫ����
�䲽�����£�
����1��ȡmg��Ʒ����ˮ���100mL��Һ��ȡ25.00mL������ƿ�У�����Һ�м�������RET��ָʾ����
����2����25.00mL��Һ�м���c mol��L-1EDTA VmL��������
����3����c1mol��L-1п����Һ���еζ����յ㣬����п����ҺV1mL��
�ٲ���2�У�����ж�EDTA��Һ�Ѽӹ�������Һ�Դ���ɫ��
�ڵζ��յ��ж�����Ϊ��Һǡ�ñ�Ϊ�ƺ�ɫ���ұ��ְ���Ӳ���ɫ��
�۸ò�Ʒ�Ĵ���Ϊ$\frac{182��cV-{c}_{1}{V}_{1}��}{m}$%��
���� ���������������п��Һ��ϣ�����������ܽ�Ƚ�С�����Կ�����������Ƴ�������������п��Һ�����ˣ�����Һ�м������̼����ɫ�����ȹ��ˣ�����Һ�м����Ҵ�����ȴ����������п�����������ᴿ����������п��
��1���Ʊ���������пʱ�������Ǹ��ֽⷴӦ���Ȼ���������ˮ���ݴ˴��⣻
��2������90�������ˮԡ���ȣ�����Ӱ�췴Ӧ���ʺ�������п���ȶ���ȷ����Ӧ���¶ȣ�
��3����������п������ˮ����������ˮ�Ҵ����ݴ��жϣ�
��4��������������п��������ˮ����������ˮ�Ҵ������Դֲ�Ʒ���ᴿ����Ϊ�ؽᾧ��������ˮ�ܽ⣬����95%�Ҵ�ϴ�ӣ�ʹ��������п������
��5���ٸ��ݷ�Ӧ��Zn-RET���ƺ�ɫ��+EDTA����ɫ���TZn-EDTA����ɫ��+BET������ɫ������EDTA����ʱ����Һ�Դ���ɫ��
����п����Һ���еζ����յ�ʱ����Һ���ɴ���ɫ��Ϊ�ƺ�ɫ��
���������֪����EDTA��Ӧ��п����Һ��п�����ʵ���Ϊc1V1��10-3mol��������ȥ��EDTA�����ʵ���Ϊc1V1��10-3mol������������п��Ӧ��EDTA�����ʵ���ΪcV��10-3mol-c1V1��10-3mol���ɼ������Ʒ����������п�����ʵ���Ϊ$\frac{100}{25}$����cV��10-3mol-c1V1��10-3mol�����ݴ˼����Ʒ�Ĵ��ȣ�
��� �⣺���������������п��Һ��ϣ�����������ܽ�Ƚ�С�����Կ�����������Ƴ�������������п��Һ�����ˣ�����Һ�м������̼����ɫ�����ȹ��ˣ�����Һ�м����Ҵ�����ȴ����������п�����������ᴿ����������п��
��1���Ʊ���������пʱ�������Ǹ��ֽⷴӦ���Ȼ���������ˮ�������ϸ��ֽⷴӦ�����������Բ������Ȼ�п��������п��
�ʴ�Ϊ�����Ȼ���������ˮ�������ϸ��ֽⷴӦ��������
��2������90�������ˮԡ���ȣ���Ӧ���¶ȹ��ͣ���Ӧ���������¶ȹ��ߣ�������п���ֽ⣬���Է�Ӧ������90��Ϻã�
�ʴ�Ϊ��ˮԡ���ȣ���Ӧ���¶ȹ��ͣ���Ӧ���������¶ȹ��ߣ�������п���ֽ⣻
��3����������п������ˮ����������ˮ�Ҵ��������ڡ���ȴ��Һ��ʱ����95%�Ҵ���Ŀ���ǽ���������п���ܽ�ȣ�����������
�ʴ�Ϊ������������п���ܽ�ȣ�����������
��4��������������п��������ˮ����������ˮ�Ҵ������Դֲ�Ʒ���ᴿ����Ϊ�ؽᾧ��������ˮ�ܽ⣬����95%�Ҵ�ϴ�ӣ�ʹ��������п��������ѡD��
�ʴ𰸣��ؽᾧ��D��
��5���ٸ��ݷ�Ӧ��Zn-RET���ƺ�ɫ��+EDTA����ɫ���TZn-EDTA����ɫ��+BET������ɫ������EDTA����ʱ����Һ�Դ���ɫ��
�ʴ�Ϊ����Һ�Դ���ɫ��
����п����Һ���еζ����յ�ʱ����Һ���ɴ���ɫ��Ϊ�ƺ�ɫ�����Եζ��յ��ж�����Ϊ��Һǡ�ñ�Ϊ�ƺ�ɫ���ұ��ְ���Ӳ���ɫ��
�ʴ�Ϊ����Һǡ�ñ�Ϊ�ƺ�ɫ���ұ��ְ���Ӳ���ɫ��
���������֪����EDTA��Ӧ��п����Һ��п�����ʵ���Ϊc1V1��10-3mol��������ȥ��EDTA�����ʵ���Ϊc1V1��10-3mol������������п��Ӧ��EDTA�����ʵ���ΪcV��10-3mol-c1V1��10-3mol���ɼ������Ʒ����������п�����ʵ���Ϊ$\frac{100}{25}$����cV��10-3mol-c1V1��10-3mol�������Բ�Ʒ�Ĵ���Ϊ$\frac{��cV��1{0}^{-3}-c1V1��1{0}^{-3}����\frac{100}{25}��455}{m}$��100%=$\frac{182��cV-{c}_{1}{V}_{1}��}{m}$%��
�ʴ�Ϊ��$\frac{182��cV-{c}_{1}{V}_{1}��}{m}$%��
���� ������������ʵ��Ʊ���������ᴿ�Ŀ��飬������ѧ���ķ���������ʵ�����������������Ŀ��飬��������ѧ�������õĿ�ѧ�������Ѷ��еȣ�

| A�� | ���³�ѹ�£�16gO2���еĺ��������Ϊ8 NA | |
| B�� | һ�������£�0.1mol����0.1mol Cl2��ַ�Ӧ��ת�Ƶĵ�����ԼΪ0.3 NA | |
| C�� | ��״���£�22.4L��ˮ����NA��NH3���� | |
| D�� | 28gC2H4�к���C-H������ĿΪ3 NA |
| A�� | CaCl2=Ca2++Cl2? | B�� | Na2SO4=Na++SO42- | ||
| C�� | HNO3=H++NO3- | D�� | NaHCO3=Na++H++CO32- |
| A�� | ��ˮ�͵⻯�ط�Ӧ��Cl2+2I-=2Cl-+I2 | |
| B�� | �������̺�������������MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2H2O+Cl2�� | |
| C�� | ������Ư�ۣ�2OH-+Cl2=Cl-+Cl0-+H2O | |
| D�� | ������ˮ��Ӧ��Cl2+H2O=H++Cl-+HClO |
| A�� | �ڰ����ڢ�A�� | B�� | �������ڢ�A�� | C�� | �������ڢ�B�� | D�� | �������ڢ�A�� |
| A�� | 6.4g��O3��O2��ɵĻ��������һ������0.4NA��ԭ�� | |
| B�� | ���³�ѹ�£�5.6g������7.1g�����г��ȼ�գ�ʧȥ�ĵ�����ĿΪ0.3NA | |
| C�� | �����£�pH=1��HNO3��Һ�к���0.1NA��H+ | |
| D�� | 0.1mol KHSO4����������������0.2NA |
| A�� | $\frac{{V}_{m}nb}{m{N}_{A}}$ | B�� | $\frac{{V}_{m}mb}{n{N}_{A}}$ | C�� | $\frac{{V}_{m}n{N}_{A}}{mb}$ | D�� | $\frac{nb{N}_{A}}{{V}_{m}m}$ |
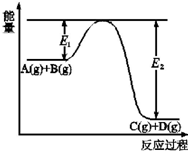 ��֪���淴ӦA��g��+B��g��?C��g��+D��g�������е�������kJ���仯��ͼ��ʾ���ش��������⣺
��֪���淴ӦA��g��+B��g��?C��g��+D��g�������е�������kJ���仯��ͼ��ʾ���ش��������⣺