题目内容
18.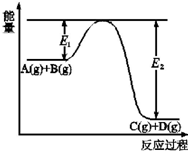 已知可逆反应A(g)+B(g)?C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题:
已知可逆反应A(g)+B(g)?C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题:(1)反应物A(g)和B(g)具有的总能量大于(填“大于”、“小于”或“等于”)生成物C(g)和D(g)具有的总能量.
(2)该反应是放热反应(填“吸热”、“放热”),△H=E2-E1(用E1和E2表示);
(3)E2表示逆反应的活化能,催化剂M能有效加快该反应的反应速率,使用催化剂M时对E1的影响是减小(填“增大”“减小”或“不变”).
分析 (1)析图象中物质能量变化可知AB反应物能量高于生成物CD,反应是放热反应;
(2)反应物能量高于生成物,反应放热;反应热等于生成物与反应物的能量差;
(3)催化剂能降低反应的活化能,加快化学反应速率.
解答 解:(1)分析图象中物质能量变化可知AB反应物能量高于生成物CD,反应是放热反应,A(g)+B(g)?C(g)+D(g)过程中的能量变化为放热,
故答案为:大于;
(2)图示反应是放热反应;反应热等于生成物的总能量与反应物总能量的差值,即E2-E1,故答案为:放热;E2-E1;
(3)E2表示逆反应的活化能;催化剂能降低反应的活化能,E1减小,故答案为:逆反应的活化能;减小.
点评 本题考查了化学反应能量变化的分析判断,影响化学平衡的因素分析,注意催化剂改变反应速率不改变化学平衡,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.设NA表示阿伏加德罗常数值,下列说法中正确的是( )
| A. | 1L1 mol•L-1 FeCl3溶液,含有Fe3+的数目为NA个 | |
| B. | 标准状况下,22.4L丙烷中碳碳共价键数目为2NA | |
| C. | 1L0.5 mol•L-1 氨水溶液中含有0.5NA个OH- | |
| D. | 室温下H2O2分解得到16 g O2,转移的电子数为2NA |
13.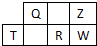 短周期元素Q、R、T、W、Z在元素周期表中的位置如图所示,其中T是该周期离子半径最小的元素,下列说法中不正确的是( )
短周期元素Q、R、T、W、Z在元素周期表中的位置如图所示,其中T是该周期离子半径最小的元素,下列说法中不正确的是( )
 短周期元素Q、R、T、W、Z在元素周期表中的位置如图所示,其中T是该周期离子半径最小的元素,下列说法中不正确的是( )
短周期元素Q、R、T、W、Z在元素周期表中的位置如图所示,其中T是该周期离子半径最小的元素,下列说法中不正确的是( )| A. | Q、Z、W可形成三原子直线型分子 | |
| B. | Z、R两元素气态氢化物的沸点:R>Z | |
| C. | Z、Q两元素的气态氢化物中键能大小:Z>Q | |
| D. | T、W两元素组成的化合物不能通过水溶液中的离子反应制取 |
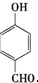 .有人提出,以对甲基苯酚为原料合成PHBA的途径如下:
.有人提出,以对甲基苯酚为原料合成PHBA的途径如下: $→_{①}^{(CH_{3})SO_{4}/OH-}$
$→_{①}^{(CH_{3})SO_{4}/OH-}$ $→_{②}^{Cl_{2}/光照}$C$→_{③}^{NaOH溶液/加热}$D$\stackrel{O_{2}、Cu/加热}{→}$EPHBA
$→_{②}^{Cl_{2}/光照}$C$→_{③}^{NaOH溶液/加热}$D$\stackrel{O_{2}、Cu/加热}{→}$EPHBA
 .
.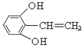 或
或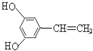 (只写一种).
(只写一种).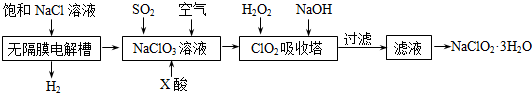

 可简写为
可简写为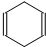 .现有某化合物W的分子结构可表示为:
.现有某化合物W的分子结构可表示为: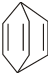 .
.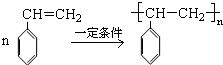 .
.