题目内容
19.常温下,将pH为8的NaOH溶液与pH为10的NaOH溶液等体积混合后,溶液的氢离子浓度最接近于( )| A. | 2×10-10mol/L | B. | $\frac{1}{2}$(10-8+10-10)mol/L | ||
| C. | (10-8+10-10)mol/L | D. | $\frac{1}{2}$(10-6+10-4) |
分析 常温下,将pH为8的NaOH溶液中c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-8}}$mol/L=10-6mol/L,pH为10的NaOH溶液c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-10}}$mol/L=10-4mol/L,二者等体积混合,则混合溶液中c(OH-)=$\frac{1{0}^{-6}+1{0}^{-4}}{2}$mol/L,溶液中c(H+)=$\frac{1{0}^{-14}}{\frac{1{0}^{-6}+1{0}^{-4}}{2}}$mol/L,据此分析解答.
解答 解:常温下,将pH为8的NaOH溶液中c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-8}}$mol/L=10-6mol/L,pH为10的NaOH溶液c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-10}}$mol/L=10-4mol/L,二者等体积混合,则混合溶液中c(OH-)=$\frac{1{0}^{-6}+1{0}^{-4}}{2}$mol/L,溶液中c(H+)=$\frac{1{0}^{-14}}{\frac{1{0}^{-6}+1{0}^{-4}}{2}}$mol/L≈2×10-10mol/L,故选A.
点评 本题考查混合溶液pH的有关计算,侧重考查学生分析计算能力,灵活利用离子积常数进行计算即可,很多同学往往选B选项而导致错误,为易错题.

练习册系列答案
相关题目
10.下列装置或操作能达到实验目的是( )
| A. | 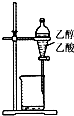 除去乙醇中的乙酸 | B. | 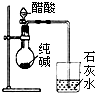 证明醋酸是弱酸 | ||
| C. | 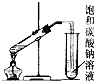 制取乙酸乙酯 | D. | 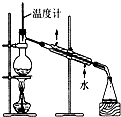 石油的分馏 |
7.将0.2mol/L的醋酸钠溶液10mL与0.1mol/L盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是( )
| A. | c(Na+)+c(H+)=c(Ac-)+c(Cl-)+c(OH-) | B. | c(HAc)>c(Cl-)>c(Ac-)>c(H+) | ||
| C. | c(Ac-)>c(Cl-)>c(HAc)>c(H+) | D. | c(Ac-)=c(Cl-)=c(HAc)>c(H+) |
14.已知N≡N键的键能是a kJ﹒mol-1,H-H键的键能是b kJ﹒mol-1,N-H键的键能是c kJ﹒mol-1,则N2(g)+3H2(g)=2NH3(g)的△H(单位:kJ﹒mol-1)为( )
| A. | 3c-a-b | B. | a+b-3c | C. | a+3b-2c | D. | a+3b-6c |
4.下列关于乙烯的说法正确的是( )
| A. | 乙烯和 2-甲基-2-戊烯无论以什么比例混合,只要总质量一定,完全燃烧后生成 CO2的质量就一定 | |
| B. | 乙烯和环丁烷(C4H8)分子间相差两个CH2原子团,故它们互为同系物 | |
| C. | 1 mol 乙烯与 Cl2完全加成后再与 Cl2发生最大程度的取代,两个过程共需 Cl26mol | |
| D. | 以乙烯为原料制备的聚乙烯可以使酸性高锰酸钾溶液褪色 |
11.瑞典皇家科学院2001年10月10日宣布,2001年诺贝尔化学奖授予在“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家.下列分子中不含有“手性碳原子”的是( )
| A. | 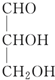 | B. | 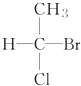 | C. | CH3CH2OH | D. | 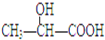 |
8.100mL浓度为2mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的量,可采用的方法是( )
| A. | 加入适量的6mol/L的盐酸 | B. | 加入数滴氯化铜溶液 | ||
| C. | 加入适量蒸馏水 | D. | 加入适量的氯化钠溶液 |
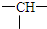 ,它可能的结构数目是( )
,它可能的结构数目是( )