题目内容
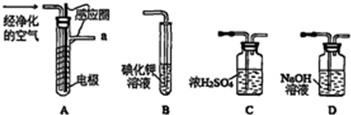
5.0.2mol有机物和0.4molO2在密闭容器中燃烧后的产物为CO2、CO和H2O(g).产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过灼热CuO充分反应后,固体质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g.0.1mol该有机物恰好与4.6g金属钠完全反应.下列关于该有机物的说法不正确的是( )| A. | 该化合物的相对分子质量是62 | |
| B. | 该化合物的化学式为C2H6O2 | |
| C. | 1mol该化合物能与2molO2发生催化氧化反应 | |
| D. | 1mol该有机物最多能与2molNa反应 |
分析 有机物燃烧生成水10.8g,其物质的量为:$\frac{10.8g}{18g/mol}$=0.6mol,设有机物燃烧生成的CO为x,则:
CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,固体减少△m
28g 16g
x 3.2g
所以x=$\frac{28g×3.2g}{16g}$=5.6g,CO的物质的量为:$\frac{5.6g}{28g/mol}$=0.2mol,
根据碳元素守恒可知CO与CuO反应生成的CO2的物质的量为0.2mol,质量为0.2mol×44g/mol=8.8g,有机物燃烧生成的CO2的质量为17.6g-8.8g=8.8g,物质的量为:$\frac{8.8g}{44g/mol}$=0.2mol,
根据碳元素守恒可知,1mol有机物含有碳原子物质的量为2mol,
根据氢元素守恒可知,1mol有机物含有氢原子物质的量为:$\frac{0.6mol×2}{0.2}$=6mol,
根据氧元素守恒可知,1mol有机物含有氧原子物质的量为:$\frac{0.6mol+0.2mol+0.2mol×2-0.4mol×2}{0.2}$=2mol,
据此可确定该有机物的分子式;0.1mol该有机物恰好与4.6g金属钠完全反应,计算出钠的物质的量,根据钠与羟基的反应关系式计算出该有机物分子中含有羟基数目,从而确定其结构.
解答 解:有机物燃烧生成水10.8g,物质的量为:$\frac{10.8g}{18g/mol}$=0.6mol,
设有机物燃烧生成的CO为x,则:
CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,固体减少△m
28g 16g
x 3.2g
所以x=$\frac{28g×3.2g}{16g}$=5.6g,CO的物质的量为:$\frac{5.6g}{28g/mol}$=0.2mol,
根据碳元素守恒可知CO与CuO反应生成的CO2的物质的量为0.2mol,质量为0.2mol×44g/mol=8.8g,有机物燃烧生成的CO2的质量为17.6g-8.8g=8.8g,物质的量为:$\frac{8.8g}{44g/mol}$=0.2mol,
根据碳元素守恒可知,1mol有机物含有碳原子物质的量为2mol,
根据氢元素守恒可知,1mol有机物含有氢原子物质的量为:$\frac{0.6mol×2}{0.2}$=6mol,
根据氧元素守恒可知,1mol有机物含有氧原子物质的量为:$\frac{0.6mol+0.2mol+0.2mol×2-0.4mol×2}{0.2}$=2mol,
所以有机物的分子式为C2H6O2,
0.1mol该有机物恰好与4.6g金属钠完全反应,4.6gNa的物质的量=$\frac{4.6g}{23g/mol}$=0.2mol,有机物与Na按物质的量之比1:2反应,有机物分子中含有羟2个-OH,该有机物的结构简式为:HOCH2CH2OH,
A.有机物的分子式为C2H6O2,相对分子质量为62,故A正确;
B.由上述分析可知,有机物的分子式为C2H6O2,故B正确;
C.该有机物的结构简式为:HOCH2CH2OH,1 mol该化合物能与1 mol O2发生催化氧化反应,故C错误;
D.0.1mol该有机物恰好与4.6g金属钠完全反应,4.6gNa的物质的量=$\frac{4.6g}{23g/mol}$=0.2mol,有机物与Na按物质的量之比1:2反应,即1 mol该有机物最多能与2 mol Na反应,故D正确;
故选C.
点评 本题考查有机物分子式的确定,题目难度中等,注意掌握利用所含元素原子守恒判断有机物的分子式的方法,明确常见有机物结构与性质为解答关键.

 名校课堂系列答案
名校课堂系列答案| A. | ①>②>③>⑤>④ | B. | ②>③>⑤>④>① | C. | ③>①>②>⑤>④ | D. | ④>⑤>②>①>③ |
| A. | 密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6kJ/mol | |
| B. | 稀醋酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5kJ/mol | |
| D. | 已知2C(s)+O2 (g)═2CO(g)△H=-221kJ/mol,则可知C的燃烧热△H=-110.5kJ/mol |
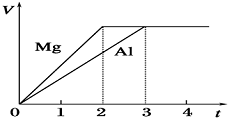 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如图所示.反应中镁和铝的( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如图所示.反应中镁和铝的( )| A. | 摩尔质量之比为2:3 | B. | 失去的电子数之比为8:9 | ||
| C. | 反应速率之比为2:3 | D. | 质量之比为4:3 |
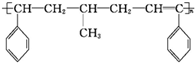 ,组成该化合物的单体可能为
,组成该化合物的单体可能为①

②CH2═CH2
③
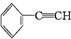
④CH2═CHCH3
⑤CH2═CH-CH═CH2
其中正确的组合是( )
| A. | ①②③ | B. | ①③④ | C. | ③④⑤ | D. | ②③⑤ |
①Na2CO3 ②Al(OH)3 ③NH4HCO3 ④Al2O3.
| A. | ①②④ | B. | ②③④ | C. | ②④ | D. | 全部 |
| A. | 白色固体,完全溶于水,得到一种无色中性溶液,此溶液导电性差 | |
| B. | 白色固体,易溶于水,得无色中性溶液,此溶液具有良好的导电性 | |
| C. | 白色固体,极易升华,如与水接触,可慢慢分解 | |
| D. | 绿色固体,易被氧化,得到一种蓝绿色溶液,此溶液具有良好的导电性 |
| A. | 标准状况下22.4L/mol 就是气体摩尔体积 | |
| B. | 非标准状况下,1mol 任何气体的体积不可能为22.4L | |
| C. | 标准状况下22.4L 任何气体都含有约6.02×1023个分子 | |
| D. | 1mol H2 和O2 的混合气体在标准状况下的体积约为44.8L |