题目内容
11.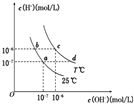 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )| A. | a点对应的溶液中大量存在:CO32-、Na+、Cl-、SO42- | |
| B. | b点对应的溶液中大量存在:Fe2+、Ba2+、K+、NO3- | |
| C. | c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Al3+ | |
| D. | d点对应的溶液中大量存在:Na+、K+、ClO-、Cl- |
分析 A.a点为25℃,c(OH-)=c(H+),溶液显中性;
B.b点为25℃,c(OH-)<c(H+),溶液显酸性;
C.c点温度高于25℃,c(OH-)=c(H+),溶液显中性;
D.d点温度高于25℃,c(OH-)>c(H+),溶液显碱性.
解答 解:A.a点为25℃,c(OH-)=c(H+),溶液显中性,CO32-在溶液中水解,溶液显示碱性,不可能大量共存,故A错误;
B.b点为25℃,c(OH-)<c(H+),溶液显酸性,Fe2+、H+、NO3-发生氧化还原反应,不能大量共存,故B错误;
C.c点温度高于25℃,c(OH-)=c(H+),溶液显中性,不能存在大量的Al3+,故C错误;
D.d点温度高于25℃,c(OH-)>c(H+),溶液显碱性,该组离子之间不反应,能大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高考常见题型,题目难度中等,侧重信息的抽取和图象分析能力的考查,把握离子之间的反应即可解答,氧化还原反应型的离子反应为解答的难点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.A、B两种元素能形成A2B2型化合物,则A和B的原子序数可能是( )
| A. | 11和8 | B. | 12和17 | C. | 11和18 | D. | 8和12 |
6. a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a是单质,b在通常状况下是气体,c、d都是氧化物,e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )
a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a是单质,b在通常状况下是气体,c、d都是氧化物,e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )
 a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a是单质,b在通常状况下是气体,c、d都是氧化物,e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )
a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a是单质,b在通常状况下是气体,c、d都是氧化物,e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )| A. | C12 | B. | N2 | C. | S | D. | C |
16.今有两种正盐的稀溶液,分别是a mol/LNaX溶液和b mol/LNaY溶液,下列说法不正确的是( )
| A. | 若a=b,pH(NaX)>pH(NaY),则相同浓度时,酸性HX<HY | |
| B. | 若a=b,并测得c(X-)=c(Y-)+c(HY),则相同浓度时,酸性HX>HY | |
| C. | 若a>b,测得c(X-)=c(Y-),则可推出溶液中c(HX)>c(HY),且相同浓度时,酸性HX<HY | |
| D. | 若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则可推出a=b=0.1 mol/L |
20.下列说法正确的是( )
| A. | 硫粉在过量的纯氧中燃烧可以生成SO3 | |
| B. | 可以用澄清石灰水鉴别SO2和CO2 | |
| C. | SO2能使酸性KMnO4水溶液褪色,是因为SO2有漂白性 | |
| D. | 铁粉与过量硫粉反应生成硫化亚铁 |
1.一定条件下在固定体积的密闭容器中,能表示反应X(g)+2Y(g)?2Z(g)一定达到化学平衡状态的是( )
| A. | X、Y、Z的物质的量之比为1:2:2 | |
| B. | X、Y、Z的浓度不再发生变化 | |
| C. | 容器中的压强不再发生变化 | |
| D. | 单位时间内生成n mol Z,同时生成2n mol Y |
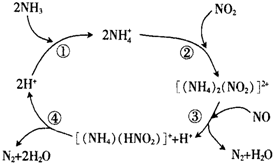 汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体.
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体.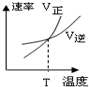
 某省2005年工业(主要是热电厂)二氧化硫排放总量为1.24×106 t,全省酸雨污染比较严重.分析降雨成分发现,雨水中阴离子仍以硫酸根离子为主,约占阴离子总量的61.9%,阳离子以铵根离子为主,约占阳离子总量的84.1%.阴离子中SO42-和NO3-的质量比为4.13:1,NO3-的比例呈明显上升的趋势.回答下列问题:
某省2005年工业(主要是热电厂)二氧化硫排放总量为1.24×106 t,全省酸雨污染比较严重.分析降雨成分发现,雨水中阴离子仍以硫酸根离子为主,约占阴离子总量的61.9%,阳离子以铵根离子为主,约占阳离子总量的84.1%.阴离子中SO42-和NO3-的质量比为4.13:1,NO3-的比例呈明显上升的趋势.回答下列问题: