题目内容
1.某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了以下实验流程图: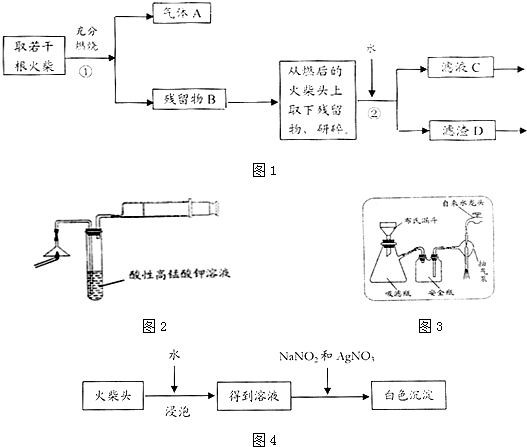
请回答以下问题:
(1)为验证气体A,按如图2所示进行实验:若能观察到KMnO4溶液(紫红色)褪色的现象,即可证明火柴头上含有S元素.
(2)写出步骤①中发生反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+O2↑、S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
(3)步骤②的实验操作装置如图3所示,该操作的名称是减压过滤(或抽滤).
(4)要证明火柴头中含有Cl元素的后续实验步骤是取滤液C,加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素.
(5)有学生提出检验火柴头上KClO3另一套实验方案:如图4所示有关的离子反应方程式为ClO3-+5Cl-+6H+═3Cl2↑+3H2O、Cl2+2I-═I2+2Cl-,有人提出上述方法中出现白色沉淀并不能充分说明火柴头上KClO3的存在,其理由是MnO2与浓盐酸共热也可产生氯气
(6)该小组猜测滤渣D对双氧水分解制氧气的速率会产生一定的影响,设计并进行了以下5次实验.
| 实验 次数 | H2O2溶液 质量分数% | H2O2溶液用量/毫升] | 物质D 用量/克 | 反应 温度/℃ | 收集气体体积/毫升 | 所需 时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
证明物质D的用量越大,反应速率越快.
分析 (1)火柴头中含有硫能燃烧,S与O2反应生成了SO2,SO2具有还原性,可用酸性高锰酸钾溶液来检验;
(2)依据火柴头上含有KClO3、MnO2、S物质的性质分析判断,氯酸钾在二氧化锰做催化剂作用分解生成氯化钾和氧气,硫单质燃烧和氧气反应生成二氧化硫气体;
(3)根据装置图可知装置名称;
(4)氯离子和酸性硝酸银溶液反应生成不溶于稀硝酸的白色沉淀;
(5)依据流程分析,氯酸钾在酸性溶液中能氧化氯离子为氯气;氯气和碘化钾反应生成碘单质,遇到淀粉变蓝;
(6)根据图表知,当其它条件都相同只有D的量不同时能证明D的用量与反应速率的关系.
解答 解:(1)从氧化还原反应角度考查SO2的检验可用KMnO4溶液,SO2具有还原性,能被KMnO4溶液氧化,
故答案为:KMnO4溶液(紫红色)褪色;
(2)步骤①中发生的与此相关的两个主要反应的方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+O2↑、S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+O2↑、S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;
(3)根据装置图可知,该装置名称是减压过滤,故答案为:减压过滤(或抽滤);
(4)氯离子和酸性硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,取滤液C,加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素,
故答案为:取滤液C,加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素;
(5)依据流程分析,氯酸钾在酸性溶液中能氧化氯离子为氯气,反应的离子方程式为:ClO3-+5Cl-+6H+═3Cl2↑+3H2O;氯气和碘化钾反应生成碘单质,反应的离子方程式为:Cl2+2I-═I2+2Cl-;碘单质遇到淀粉变蓝;上述方法中出现的现象并不能充分说明火柴头上有KClO3的存在,因为二氧化锰和浓盐酸加热也发生反应生成氯气,
故答案为:ClO3-+5Cl-+6H+═3Cl2↑+3H2O、Cl2+2I-═I2+2Cl-;MnO2与浓盐酸共热也可产生氯气;
(6)据图表知,当其它条件都相同只有D的量不同时能证明D的用量与反应速率的关系,则实验②和③能证明证明物质D的用量越大,反应速率越快,实验①和⑤能证明温度越高,反应速率越快;实验②和④证明H2O2的质量分数越大,反应速率越快,
故答案为:①;⑤;②;③.
点评 本题考查了物质现在的实验分析验证和实验基本操作,物质性质的理解应用时解题关键,题目难度中等.

| A. | CaCO3 | B. | NH4HCO3 | C. | Na2CO3 | D. | NH4Cl |
| A. | 铝离子 | B. | 氢氧化铝 | ||
| C. | 四羟基合铝酸根离子 | D. | 铝离子和氢氧化铝 |
| A. | 能使酚酞试液变红的溶液中:Na+、Cl-、SO42-、Fe3+ | |
| B. | c(H+):c(OH-)=105:1的溶液中:K+、HCO3-、Cl-、Na+ | |
| C. | c(H+)=1.0×10-13mol•L-1的溶液中:Na+、SO42-、Al(OH)4-、CO32- | |
| D. | 强酸性溶液中:NH4+、I-、Fe2+、NO3- |
(1)Br位于元素周期表第四周期第VIIA族;Na和O形成1:1的化合物的电子式:
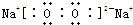 .该物质含有的化学键为:离子键和非极性键.
.该物质含有的化学键为:离子键和非极性键.(2)用“>”或“<”填空:
| 稳定性 | 粒子半径 | 熔点 | 键的极性 |
| NH3<H2O | O2-> Mg2+ | SO3< Na2O2 | H-O> H-N |
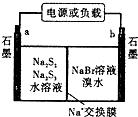
①放电时Na+向b极迁移(填“a或b,”).
②放电时负极的电极反应式为:3S22--2e-=2S32-
(4)已知N4为正四面体结构,N-N键能为167kJ•mol-1,N≡N键能为942kJ•mol-1.写出N4(g)转化为N2(g)的热化学方程式N4(g)=2N2(g)△H=-882kJ/mol.
| A. | 1mol•L-1CaCl2溶液中所含Ca2+离子的数目为NA | |
| B. | 100g质量分数为36.5%的浓盐酸中所含HCl分子数为NA | |
| C. | 标况下,11.2LBr2含有的分子数为0.5 NA | |
| D. | 4.6gNa与100mL含0.1molHCl的盐酸溶液反应,转移电子数目为0.2NA |
①硫酸钾②甲醛③氯酸钾④硝酸汞⑤氯化铵⑥氢氧化钠.
| A. | ②④⑥ | B. | ①③⑤ | C. | ①②③ | D. | ④⑤⑥ |