ЬтФПФкШн
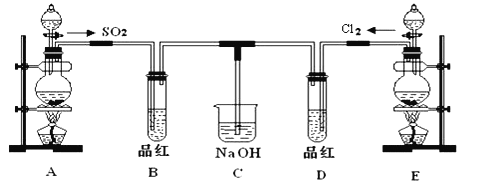
ЁОЬтФПЁПЪЕбщЪвгУЭМЪОзАжУжЦШЁИЩдяЕФАБЦјЃК
ЃЈ1ЃЉЪЕбщЪвжЦБИАБЦјЛЏбЇЗНГЬЪНЪЧ_______________________________ЁЃ
ЃЈ2ЃЉЙЄвЕжЦБИАБЦјЕФЛЏбЇЗНГЬЪНЪЧ_____________________________________________ЁЃ
ЃЈ3ЃЉШєЯыжЦЕУИЩдяЕФАБЦјЃЌгІбЁдёзАжУ_______ЃЈЬюЁАМзЁБЁАввЁБЛђЁАБћЁБЃЉЃЌВЛФмгУввзАжУИЩдяАБЦјЕФдвђ_______________________________ЃЈгУЛЏбЇЗНГЬЪНБэЪОЃЉЁЃ
ЃЈ4ЃЉМьбщЪдЙмCжаАБЦјЪеМЏТњЕФЗНЗЈЪЧ______________________ЁЃ
ЃЈ5ЃЉЪдЙмПкЗХжУУоЛЈЕФзїгУЪЧ_________________________________________ЁЃ
ЃЈ6ЃЉФГЭЌбЇЩшМЦСЫШчЭМзАжУЪеМЏАБЦјЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ________(ЬюзжФИ)ЁЃ
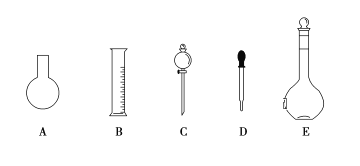
AЃЎЪеМЏАБЦјЕФдРэЪЧЯђЯТХХПеЦјЗЈ
BЃЎИЩдяЙмЕФзїгУЪЧЗРжЙЕЙЮќ
CЃЎЕБЩеБжаЕФЫЎБфКьЪБжЄУїАБЦјвбЪеМЏТњ
DЃЎИУзАжУЛсаЮГЩКьЩЋХчШЊ
ЁОД№АИЁП2NH4Cl+Ca(OH)2![]() CaCl2+2NH3Ёќ+H2O N2+3H2
CaCl2+2NH3Ёќ+H2O N2+3H2![]() 2NH3 Бћ 2NH3+H2SO4=(NH4)2SO4 гУЪЊШѓЕФКьЩЋЪЏШяЪджНППНќЪдЙмПкЃЌШєЪджНБфРЖЃЌдђЫЕУївбЪеМЏТњЃЈЛђгУВЃСЇАєеКШЁХЈбЮЫсППНќЪдЙмПкЃЌШєгаАзбЬЩњГЩЃЌдђЫЕУївбЪеМЏТњЃЉ ЗРжЙПеЦјгыАБЦјЖдСїЃЌЪеМЏВЛЕНДПОЛЕФАБЦј D
2NH3 Бћ 2NH3+H2SO4=(NH4)2SO4 гУЪЊШѓЕФКьЩЋЪЏШяЪджНППНќЪдЙмПкЃЌШєЪджНБфРЖЃЌдђЫЕУївбЪеМЏТњЃЈЛђгУВЃСЇАєеКШЁХЈбЮЫсППНќЪдЙмПкЃЌШєгаАзбЬЩњГЩЃЌдђЫЕУївбЪеМЏТњЃЉ ЗРжЙПеЦјгыАБЦјЖдСїЃЌЪеМЏВЛЕНДПОЛЕФАБЦј D
ЁОНтЮіЁП
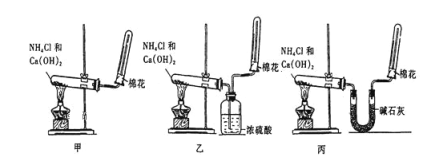
ЃЈ1ЃЉЪЕбщЪвЪЧРћгУЙЬЬхЧтбѕЛЏИЦгыТШЛЏяЇжЦБИАБЦјЃЛ
ЃЈ2ЃЉЙЄвЕЩЯРћгУЕЊЦјгыЧтЦјжЦБИАБЦјЃЛ
ЃЈ3ЃЉАБЦјЮЊМюадЦјЬхЃЌВЛФмгУЫсадИЩдяМСИЩдяЃЛ
ЃЈ4ЃЉвРОнАБЦјЪЧМюадЦјЬхЃЌгіЕНЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЃЈЛђгіЕНеКгаХЈбЮЫсЕФВЃСЇАєЃЌУААзбЬЃЉМьбщЪЧЗёМЏТњЃЛ
ЃЈ5ЃЉАБЦјУмЖШБШПеЦјаЁЃЌЪеМЏАБЦјЪБКмШнвзгЩгкжмЮЇПеЦјЕФСїЖЏ,ЪЙЪеМЏзАжУВЛФмМЏТњЃЛ
ЃЈ6ЃЉAЃЎАБЦјЕФУмЖШаЁгкПеЦјУмЖШЃЛ
BЃЎгаЛКГхзїгУЕФзАжУФмЗРжЙЕЙЮќЃЛ
CЃЎАБЫЎШмвКГЪМюадЃЌМюгіЗгЬЊЪдвКБфКьЩЋЃЛ
DЃЎИЩдяЙмгаЛКГхзїгУЃЌВЛФмаЮГЩХчШЊЁЃ
ЃЈ1ЃЉЪЕбщЪвРћгУNH4ClКЭCaЃЈOHЃЉ2МгШШПЩжЦБИАБЦјЃЌЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК2NH4Cl+Ca(OH)2![]() CaCl2+2NH3Ёќ+H2OЃЌ
CaCl2+2NH3Ёќ+H2OЃЌ
ЙЪД№АИЮЊЃК2NH4Cl+Ca(OH)2![]() CaCl2+2NH3Ёќ+H2OЃЛ
CaCl2+2NH3Ёќ+H2OЃЛ
ЃЈ2ЃЉЙЄвЕЩЯРћгУЕЊЦјгыЧтЦјКЯГЩАБЃЌЦфЛЏбЇЗНГЬЪНЮЊЃКN2+3H2![]() 2NH3ЃЌ
2NH3ЃЌ
ЙЪД№АИЮЊЃКN2+3H2![]() 2NH3ЃЛ
2NH3ЃЛ
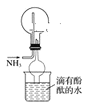
ЃЈ3ЃЉАБЦјЮЊМюадЦјЬхЃЌИљОнЭМЪОаХЯЂЃЌПЩбЁБћМюадИЩдяМСЃЈМюЪЏЛвЃЉИЩдяЃЌЖјВЛФмгУзАжУввЃЌвђЮЊХЈСђЫсЮЊЫсадИЩдяМСЃЌЛсгыАБЦјЗЂЩњЛЏбЇЗДгІЩњГЩСђЫсяЇЃЌЦфЛЏбЇЗНГЬЪНЮЊЃК2NH3+H2SO4=(NH4)2SO4ЃЌ
ЙЪД№АИЮЊЃКБћЃЛ2NH3+H2SO4=(NH4)2SO4ЃЛ
ЃЈ4ЃЉАБЦјЪЧМюадЦјЬхЃЌгіЕНЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖжЄУїМЏТњЛђеКгаХЈбЮЫсЕФВЃСЇАєЃЌУААзбЬЃЌЙЪМьбщЪдЙмCжаАБЦјЪеМЏТњЕФЗНЗЈЮЊЃКгУЪЊШѓЕФКьЩЋЪЏШяЪджНППНќЪдЙмПкЃЌШєЪджНБфРЖЃЌдђЫЕУївбЪеМЏТњЃЈЛђгУВЃСЇАєеКШЁХЈбЮЫсППНќЪдЙмПкЃЌШєгаАзбЬЩњГЩЃЌдђЫЕУївбЪеМЏТњЃЉЃЌ
ЙЪД№АИЮЊЃКгУЪЊШѓЕФКьЩЋЪЏШяЪджНППНќЪдЙмПкЃЌШєЪджНБфРЖЃЌдђЫЕУївбЪеМЏТњЃЈЛђгУВЃСЇАєеКШЁХЈбЮЫсППНќЪдЙмПкЃЌШєгаАзбЬЩњГЩЃЌдђЫЕУївбЪеМЏТњЃЉЃЛ
ЃЈ5ЃЉЮЊЗРжЙПеЦјЖдСїЃЌЗРжЙЪеМЏЕФАБЦјВЛДПЃЌашвЊдкЪдЙмПкШћвЛЭХУоЛЈЃЌЙЪЪдЙмПкЗХжУУоЛЈЕФзїгУЪЧЗРжЙПеЦјгыАБЦјЖдСїЃЌЪеМЏВЛЕНДПОЛЕФАБЦјЃЌ
ЙЪД№АИЮЊЃКЗРжЙПеЦјгыАБЦјЖдСїЃЌЪеМЏВЛЕНДПОЛЕФАБЦјЃЛ
ЃЈ6ЃЉAЃЎАБЦјЕФУмЖШаЁгкПеЦјУмЖШЃЌЧвКЭбѕЦјВЛЗДгІЃЌЫљвдЪеМЏАБЦјПЩвдВЩгУЯђЯТХХПеЦјЗЈЪеМЏЃЌЙЪAЯюе§ШЗЃЛ
BЃЎИЩдяЙмгаЛКГхзїгУЃЌЫљвдФмЗРжЙЕЙЮќЃЌЙЪBЯюе§ШЗЃЛ
CЃЎАБЫЎКЭЫЎЗДгІЩњГЩвЛЫЎКЯАБЃЌвЛЫЎКЯАБФмЕчРыГіЧтбѕИљРызгЖјЪЙЦфШмвКГЪМюадЃЌМюгіЗгЬЊЪдвКБфКьЩЋЃЌЙЪCЯюе§ШЗЃЛ
DЃЎИЩдяЙмгаЛКГхзїгУЃЌЩеБжавКЬхВЛФмНјШыЩеЦПжаЃЌЫљвдВЛФмаЮГЩКьЩЋХчШЊЃЌЙЪDЯюДэЮѓЃЛ
Д№АИЮЊDЁЃ

 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИЁОЬтФПЁПЬМКЭЬМЕФЛЏКЯЮядкЩњВњЁЂЩњЛюжаЕФгІгУЗЧГЃЙуЗКЁЃ ЯжНЋВЛЭЌСПЕФCO2ЃЈgЃЉКЭH2ЃЈgЃЉЗжБ№ЭЈШыЬхЛ§ЮЊ2LЕФКуШнУмБеШнЦїжаЃЌНјааШчЯТЗДгІЃКCO2(gЃЉ+H2ЃЈgЃЉ![]() [Failed to download image : ]COЃЈgЃЉ+H2OЃЈgЃЉЃЌЕУЕНШчЯТШ§зщЪ§ОнЃК
[Failed to download image : ]COЃЈgЃЉ+H2OЃЈgЃЉЃЌЕУЕНШчЯТШ§зщЪ§ОнЃК
ЪЕбщзщ | ЮТЖШ/Ёц | Ц№ЪМСП/mol | ЦНКтСП/mol | ДяЕНЦНКтЫљашЪБМф/min | |
CO2 | H2 | CO | |||
1 | 800 | 4 | 2.5 | 1.5 | 5 |
2 | 830 | 2 | 2 | 1 | 3 |
3 | 830 | 2 | 2 | 1 | 1 |

ЃЈ1ЃЉЪЕбщ1жаЃЌЦНКтГЃЪ§K=0.9ЃЛvЃЈH2ЃЉ=0.15mol/ЃЈLminЃЉИУЗДгІЕФе§ЗДгІЮЊ______ЃЈЬюЁАЮќЁБЛђЁАЗХЁБЃЉШШЗДгІЃЛ
ЃЈ2ЃЉЪЕбщ3ИњЪЕбщ2ЯрБШЃЌИФБфЕФЬѕМўПЩФмЪЧ___________________________
ЃЈД№вЛжжЧщПіМДПЩЃЉЃЛШєИУЗДгІЗћКЯЭМЫљЪОЕФЙиЯЕЃЌдђдкЭМжаYжсБэЪО___________________________
ЃЈ3ЃЉФмХаЖЯИУЗДгІДяЕНЛЏбЇЦНКтзДЬЌЕФвРОнЪЧ______ЃЈЖрбЁПлЗжЃЉЃЎ
aЃЎШнЦїжабЙЧПВЛБф bЃЎЛьКЯЦјЬхжаcЃЈCO ЃЉВЛБф
cЃЎvЃЈH2ЃЉе§=vЃЈH2OЃЉФц dЃЎcЃЈCO2ЃЉ=cЃЈCOЃЉ
ЃЈ4ЃЉФГЮТЖШЯТЃЌЦНКтХЈЖШЗћКЯЯТЪНЃКcЃЈCO2ЃЉcЃЈH2ЃЉ=cЃЈCOЃЉcЃЈH2OЃЉгЩДЫПЩвдХаЖЯДЫЪБЕФЮТЖШЮЊ______ЃЎЦфЫќЬѕМўВЛБфЃЌЩ§ИпЮТЖШЃЌдЛЏбЇЦНКтЯђ______ЗДгІЗНЯђвЦЖЏЃЈЬюЁАе§ЁБЛђЁАФцЁБЃЉЃЌШнЦїФкЛьКЯЦјЬхЕФУмЖШ______ЃЈЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБЃЉЃЎ
ЃЈ5ЃЉ