题目内容
【题目】A、B、C、D、E、F、G七种短周期元素,其原子序数依次增大。A的原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是内层电子数的3倍;D与G处在同一族;F是地壳中含量最高的金属元素。请回答下列问题:
(1)元素F在周期表中的位置 。
(2)B、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(3)配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于 (填晶体类型)。
(4)CA3分子的电子式为 。
(5)ED是优良的耐高温材料,其晶体结构与NaCl晶体相似。ED的熔点比NaCl高,其原因是 。
(6)由A、D、G中任两种元素构成甲、乙两种均含18个电子的分子,所含原子的数目依次为3、4。则甲分子的中心原子采取 杂化;1 mol乙分子含有 molσ键。
【答案】(1)第三周期第ⅢA族 (2)N > O > C (3)分子晶体 (4)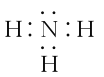
(5)MgO晶体中离子的电荷数大于NaCl,离子间的平均距离小于NaCl,离子键的键能
更大,熔点更高(晶格能大)(6)①sp3 ②3mol
【解析】
试题分析:A的原子中没有成对电子,则A是H元素,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,则B是碳元素,D原子最外层电子数是内层电子数的3倍,D是氧元素,D与G处在同一族,G是硫元素,由于原子序数递增,则C是N元素,F是地壳中含量最高的金属元素,则F是铝元素;
(1)元素F在周期表中的位置为第三周期第ⅢA族;
(2)N原子最外层p电子半满,为稳定结构,非金属性强的第一电离能大,则第一电离能由大到小的顺序为N>O>C;
(3)因为Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,根据相似相溶原理,固态Ni(CO)4属于分子晶体;
(4)氨气分子的电子式为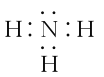 ;
;
(5)ED是优良的耐高温材料,其晶体结构与NaCl晶体相似,则ED是MgO,MgO晶体中离子的电荷数大于NaCl,离子间的平均距离小于NaCl,离子键的键能更大,熔点更高(晶格能大);
(6)由H、O、S中任两种元素构成甲、乙两种均含18个电子的分子,所含原子的数目依次为3、4,所以甲是硫化氢、乙是过氧化氢,硫化氢中硫是sp3杂化;1mol过氧化氢分子含有3molσ键。