题目内容
【题目】无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1,主要步骤如下:

图1 图2
步骤1、三颈瓶中装入10g镁屑和150mL无水乙醚;装置B中加入15mL液溴;
步骤2、缓慢通入干燥的氮气,直至溴完全导入三颈瓶中;
步骤3、反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品;
步骤4、室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg与Br2反应剧烈放热;MgBr2具有强吸水性;
②MgBr2+3C2H5OC2H5![]() MgBr23C2H5OC2H5
MgBr23C2H5OC2H5
请回答:
(1)仪器A的名称是______;
(2)实验中不能用干燥空气代替干燥N2,原因是______________;
(3)步骤3中,第一次过滤除去的物质是_________________;
(4)有关步骤4的说法,正确的是__________________;
A.可用95%的乙醇代替苯溶解粗品 B.洗涤晶体可选用0℃的苯
C.加热至160℃的主要目的是除去苯 D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y)标准溶液滴定,反应的离子方程式:Mg2++Y4﹣═MgY2
①滴定管洗涤前的操作是_______________________;
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500molL﹣1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液25.00mL,则测得无水MgBr2产品的纯度是__________(以质量分数表示)。
【答案】干燥管 防止镁屑与氧气反应,生成的MgO阻碍Mg和Br2的反应 镁屑 BD 检漏 92%
【解析】
(1)根据装置图,结合常见仪器的结构回答;
(2)实验中使用了镁屑,结合镁的化学性质分析解答;
(3)根据实验步骤,结合涉及物质的性质分析判断;
(4)根据溴化镁有强烈的吸水性,结合题干实验步骤分析解答;
(5)①根据滴定管的使用注意事项分析判断;②依据方程式Mg2++Y4-═MgY2-,计算出溴化镁的物质的量和质量,再计算溴化镁的产品的纯度。
(1)根据装置图,仪器A为干燥管,故答案为:干燥管;
(2)本实验要用镁屑和液溴反应生成溴化镁,所以装置中不能有能与镁反应的气体,例如氧气,所以不能用干燥的空气代替干燥的氮气,故答案为:防止镁屑与氧气反应生成的氧化镁阻碍Mg和Br2的反应;
(3)步骤3过滤出去的是不溶于水的镁屑,故答案为:镁屑;
(4)A.95%的乙醇中含有水,溴化镁有强烈的吸水性,故A错误;B.加入苯的目的是除去乙醚和溴,洗涤晶体用0°C的苯,可以减少产品的溶解,故B正确;C.加热至160°C的主要目的是分解三乙醚合溴化镁得到溴化镁,不是为了除去苯,故C错误;D.该步骤是为了除去乙醚和溴,故D正确;故答案为:BD;
(5)①滴定管使用前需要检查滴定管是否漏液,因此洗涤前的操作是,故答案为:检漏;
②依据方程式Mg2++Y4-═MgY2-分析,溴化镁的物质的量=0.0500mol/L×0.025L=0.00125mol,则溴化镁的质量为0.00125mol×184g/mol=0.23g,溴化镁的产品的纯度=![]() ×100%=92%,故答案为:92%。
×100%=92%,故答案为:92%。

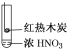
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应