题目内容
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是
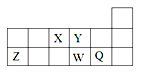
A. 离子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)>r(Z3+)
B. 元素W的最高价氧化物对应水化物的酸性比Q的强
C. 元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键
D. X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应
【答案】B
【解析】试题分析:电子层数越多半径越大,电子层数相同时,质子数越多半径越小,离子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)>r(Z3+),故A正确;同周期从左到右元素非金属性增强,最高价氧化物对应水化物的酸性增强,元素Q的最高价氧化物对应水化物的酸性比W的强,故B错误;元素X的氢化物是氨气、Q的氢化物是氯化氢,化合的产物是氯化铵,既含共价键又含离子键,故C正确;X、Z、W、Q四种元素的最高价氧化物对应水化物分别是硝酸、氢氧化铝、硫酸、高氯酸均能与强碱反应,故D正确。

【题目】甲、乙组同学分别做了以下探究实验。
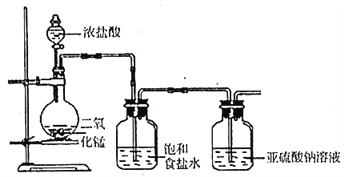
(1)甲组探究Cl2与Na2SO3溶液反应,实验装置如下。
①写出制取氯气的化学方程式______________。
②该装置的不足之处除无尾气吸收装置外,另一处是______________。
③Cl2与Na2SO3溶液反应的离子方程式为____________。
④设计实验,简述实验步骤,证明洗气瓶中的Na2SO3已被氧化_________。
(2)乙组探究乙酸乙酯在不同温度、不同浓度NaOH溶液中的水解速率。取四只大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积来确定水解反应的速率
实验试剂 | 试管I | 试管II | 试管Ⅲ | 试管IV |
乙酸乙酯/mL | 1 | V1 | V2 | V3 |
1mol/LNaOH/mL | V4 | 3 | 0 | V5 |
蒸馏水/mL | 0 | V6 | 5 | 2 |
⑤请完成上表,其中V2=______,V4=______,V5=_______。
⑥实验中,可用饱和食盐水替代蒸馏水,以减小乙酸乙酯在水中的溶解度,使实验结果更准确;但不能用饱和Na2CO3溶液替代蒸馏水,其原因是____;实验中,试管IV比试管II中的酯层减少更快,其原因有:温度高速率快,还可能有_________。 (乙酸乙酯沸点为77.1℃)