题目内容
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。
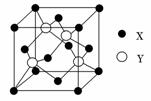
①在1个晶胞中,X离子的数目为________。
②该化合物的化学式为________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是________。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是________。
(4)Y与Z可形成YZ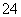 。
。
①YZ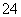 的空间构型为________(用文字描述)。
的空间构型为________(用文字描述)。
②写出一种与YZ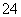 互为等电子体的分子的化学式:________。
互为等电子体的分子的化学式:________。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________。
解析:本题主要考查原子结构与性质知识,意在考查考生的空间想象能力及对物质结构和性质的理解能力。X的核外电子排布式为1s22s22p63s23p63d104s2,X为Zn;Y的核外电子排布式为1s22s22p63s23p4,Y为S;根据Z的信息可知Z为O。(1)①由晶胞结构可知,X分别位于晶胞的顶点和面心,根据晶胞中原子的“分摊法” 可计算一个晶胞中的X原子数为:8×1/8+6×1/2=4。②Y原子全部在晶胞中,故一个晶胞中含有4个Y原子。故该化合物的化学式为ZnS。(2)H2S分子中S原子有两对成键电子和两对孤对电子,所以H2S分子中S原子的轨道杂化类型为sp3杂化。(3)H2O与乙醇可以形成分子间氢键,使得水与乙醇互溶;而H2S与乙醇不能形成分子间氢键,故H2S在乙醇中的溶解度小于H2O。(4)①SO
可计算一个晶胞中的X原子数为:8×1/8+6×1/2=4。②Y原子全部在晶胞中,故一个晶胞中含有4个Y原子。故该化合物的化学式为ZnS。(2)H2S分子中S原子有两对成键电子和两对孤对电子,所以H2S分子中S原子的轨道杂化类型为sp3杂化。(3)H2O与乙醇可以形成分子间氢键,使得水与乙醇互溶;而H2S与乙醇不能形成分子间氢键,故H2S在乙醇中的溶解度小于H2O。(4)①SO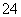 的中心原子S周围有4对成键电子,形成以S为体心,O为顶点的正四面体结构;②SO
的中心原子S周围有4对成键电子,形成以S为体心,O为顶点的正四面体结构;②SO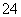 中S、O最外层均为6个电子,故SO
中S、O最外层均为6个电子,故SO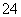 中原子最外层共有32个电子;CCl4、SiCl4中原子的最外层电子总数均为4+7×4=32,故SO
中原子最外层共有32个电子;CCl4、SiCl4中原子的最外层电子总数均为4+7×4=32,故SO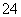 、CCl4、SiCl4为等电子体。(5)[Zn(NH3)4]Cl2中[Zn(NH3)4]2+与Cl-形成离子键,而[Zn(NH3)4]2+中含有4个Zn—N键(配位键)和12个N—H键,共16个共价单键,故1 mol该配合物中含有16 mol σ键。
、CCl4、SiCl4为等电子体。(5)[Zn(NH3)4]Cl2中[Zn(NH3)4]2+与Cl-形成离子键,而[Zn(NH3)4]2+中含有4个Zn—N键(配位键)和12个N—H键,共16个共价单键,故1 mol该配合物中含有16 mol σ键。
答案:(1)①4 ②ZnS
(2)sp3
(3 )水分子与乙醇
)水分子与乙醇 分子之间形成氢键
分子之间形成氢键
(4)①正四面体 ②CCl4或SiCl4等
(5)16NA或16×6.02×1023个

 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
 B.2H2(g)+O2(g)=2H2O(1) △H<0
B.2H2(g)+O2(g)=2H2O(1) △H<0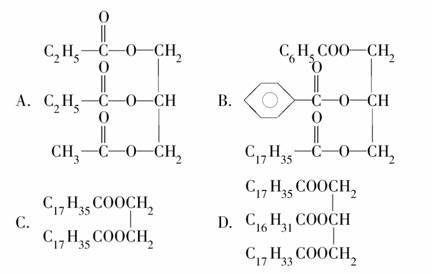
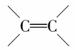 ,称为二十六碳六烯酸,则其甘油酯的结构简式为
,称为二十六碳六烯酸,则其甘油酯的结构简式为 A.镓的金属性比铝弱 B.镓的常见化合价为+3
A.镓的金属性比铝弱 B.镓的常见化合价为+3