题目内容
 (1)甲烷也是一种清洁燃料,但不完全燃烧时热效率降低并会产生有毒气体造成污染.
(1)甲烷也是一种清洁燃料,但不完全燃烧时热效率降低并会产生有毒气体造成污染.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ/mol
2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ/mol
则甲烷不完全燃烧生成一氧化碳和液态水时的热效率只是完全燃烧时的
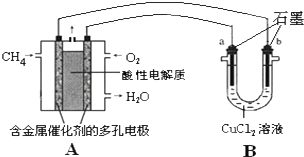
(2)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:请回答:
①甲烷燃料电池的负极反应式是
②当线路中有0.1mol电子通过时,
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)根据盖斯定律计算甲烷不完全燃烧放出的热量,与其完全燃烧放出的热量比较得出热效率;
(2)①甲烷燃料酸性电池中,负极上甲烷失电子和水生成氢离子和二氧化碳;
②b电极为阴极,阴极上铜离子放电生成Cu,根据Cu和转移电子之间的关系式计算.
(2)①甲烷燃料酸性电池中,负极上甲烷失电子和水生成氢离子和二氧化碳;
②b电极为阴极,阴极上铜离子放电生成Cu,根据Cu和转移电子之间的关系式计算.
解答:
解:(1)CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ/mol①
2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ/mol②
将方程式①×2-②得2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H=(-890.3kJ/mol)×2-(-566.0kJ/mol)=-1214.6kJ/mol,所以
甲烷不完全燃烧热化学反应方程式为2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H=-1214.6kJ/mol,甲烷不完全燃烧生成一氧化碳和液态水时的热效率只是完全燃烧时倍数=
=0.7,故答案为:0.7;
(2)①甲烷燃料酸性电池中,负极上甲烷失电子和水生成氢离子和二氧化碳,电极反应为CH4-8e─+2H2O=CO2+8H+,故答案为:CH4-8e─+2H2O=CO2+8H+;
②b电极为阴极,阴极上铜离子放电生成Cu,根据Cu和转移电子之间的关系式得析出Cu的质量=
×1×64g/mol=3.2g,故答案为:b;3.2.
2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ/mol②
将方程式①×2-②得2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H=(-890.3kJ/mol)×2-(-566.0kJ/mol)=-1214.6kJ/mol,所以
甲烷不完全燃烧热化学反应方程式为2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H=-1214.6kJ/mol,甲烷不完全燃烧生成一氧化碳和液态水时的热效率只是完全燃烧时倍数=
| 1214.6 |
| 1780.6 |
(2)①甲烷燃料酸性电池中,负极上甲烷失电子和水生成氢离子和二氧化碳,电极反应为CH4-8e─+2H2O=CO2+8H+,故答案为:CH4-8e─+2H2O=CO2+8H+;
②b电极为阴极,阴极上铜离子放电生成Cu,根据Cu和转移电子之间的关系式得析出Cu的质量=
| 0.1mol |
| 2 |
点评:本题考查了原电池原理和电解池原理,涉及盖斯定律、电极反应式的书写等知识点,难点是电极反应式的书写,要结合电解质溶液酸碱性书写,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有等体积的NaCl、CaCl2、AlCl3溶液,完全沉淀其中的Cl-消耗同浓度的AgNO3溶液体积相等,则三种溶质的浓度之比为( )
| A、1:1:1 |
| B、1:2:3 |
| C、6:3:2 |
| D、3:2:1 |
下列说法正确的是( )
| A、水泥、玻璃、陶瓷、水晶都属于硅酸盐产品 |
| B、二氧化碳通入水玻璃可以得到硅酸 |
| C、因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以酸性硅酸比碳酸强 |
| D、可以用澄清石灰水鉴别SO2和CO2 |