题目内容
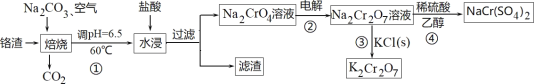
【题目】利用含铬废料(主要含 Cr2O3,还含有 FeO、SiO2、Al2O3 等杂质)制备重铬酸钠,实现清洁化工生产,工艺流程如图:
回答下列问题:
(1)焙烧 Cr2O3 转化为Na2CrO4 的化学反应方程式是_____;
(2)实验室模拟此工业流程①,控制反应温度 60℃的方法是_____;
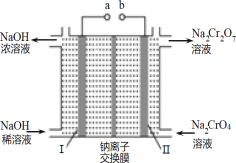
(3)流程②用石墨做电极电解 Na2CrO4 溶液,制备Na2Cr2O7,其原理如图所示,a 是_____极;电极Ⅱ的电极反应式是_____;当生成 2mol Na2Cr2O7时,电路中转移的电子_____mol;
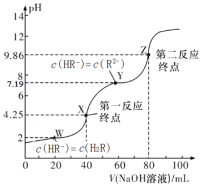
(4)由下图和下表中的溶解度变化,流程③制备 K2Cr2O7,应先充分加热,然后_____反应才能顺利进行;

重铬酸钠的溶解度表:
温度℃ | 10 | 20 | 40 | 60 | 80 | 100 |
溶解度% | 61.6 | 62.8 | 65.1 | 71.8 | 78.7 | 81.1 |
(5)为进一步减少制得的 K2Cr2O7 晶体中 NaCl 等杂质,应再进行_____操作;
(6)流程④Na2Cr2O7 溶液与乙醇反应,乙醇可能被氧化为_____(写一种即可)。
【答案】2Cr2O3+4Na2CO3+3O2 ![]() 4Na2CrO4+4CO2 水浴加热 负极 4OH-―4e-=2H2O+O2↑或2H2O-4e-=O2↑+4H+ 4 冷却结晶(降低温度) 重结晶 乙醛(CH3CHO)、乙酸(CH3COOH)、二氧化碳(CO2)等
4Na2CrO4+4CO2 水浴加热 负极 4OH-―4e-=2H2O+O2↑或2H2O-4e-=O2↑+4H+ 4 冷却结晶(降低温度) 重结晶 乙醛(CH3CHO)、乙酸(CH3COOH)、二氧化碳(CO2)等
【解析】
利用含铬废料(主要含 Cr2O3,还含有 FeO、SiO2、Al2O3 等杂质)制备重铬酸钠。将铬铁矿和碳酸钠、空气混合焙烧,发生反应得到Na2CrO4、NaAlO2、Na2SiO3等和CO2,然后在60℃时调节溶液的pH=6.5,用盐酸浸取后过滤,得到的滤渣中主要含有硅酸、氢氧化铁、氢氧化铝等,滤液中含有Na2CrO4和NaCl,然后用石墨做电极电解 Na2CrO4 溶液,制备Na2Cr2O7,在Na2Cr2O7溶液中加入氯化钾固体可以制得K2Cr2O7,在Na2Cr2O7溶液中加入稀硫酸和乙醇,可以制得Na Cr(SO4)2,据此分析解答。
(1)Cr2O3 与碳酸钠在空气中焙烧反应生成Na2CrO4 的化学反应方程式为2Cr2O3+4Na2CO3+3O2 ![]() 4Na2CrO4+4CO2,故答案为:2Cr2O3+4Na2CO3+3O2
4Na2CrO4+4CO2,故答案为:2Cr2O3+4Na2CO3+3O2 ![]() 4Na2CrO4+4CO2;
4Na2CrO4+4CO2;
(2)可以采用水浴加热的方法,控制反应温度 60℃,故答案为:水浴加热;
(3)Na2CrO4 溶液中存在2CrO42-+2H+Cr2O72-+H2O,用图示装置(均为石墨电极)电解Na2CrO4溶液制取Na2Cr2O7,需要通过电解生成H+提高溶液的酸性,说明该电极(电极Ⅱ)是阳极,连接电源的正极,即b为正极,则a为负极;电极Ⅱ为阳极,溶液中氢氧根离子失电子生成氧气,电极反应式为4OH--4e-=2H2O+O2↑或2H2O-4e-=O2↑+4H+;由CrO42-+2H +=Cr2O72-+H2O可知,每生成2molNa2Cr2O7时,理论上II电极生成4molH+,根据阳极反应式4OH--4e-=2H2O+O2↑可知,每生成4molH+,转移4mol电子,故答案为:负极;4OH-―4e-=2H2O+O2↑或2H2O-4e-=O2↑+4H+;4;
(4) 根据溶解度曲线和重铬酸钠的溶解度表可知,K2Cr2O7的溶解度随温度的变化较大,而Na2Cr2O7的溶解度受温度的影响不大,且温度较低是由水中的溶解度:Na2Cr2O7>K2Cr2O7,因此流程③中向Na2Cr2O7溶液中加入适量KCl,充分加热,蒸发浓缩至表面出现晶膜,然后冷却结晶,析出K2Cr2O7固体,反应才能顺利进行,故答案为:冷却结晶(降低温度);
(5) 根据溶解度曲线,K2Cr2O7的溶解度随温度的变化较大,而氯化钠的溶解度受温度的影响不大,为进一步减少制得的 K2Cr2O7 晶体中 NaCl 等杂质,需要对K2Cr2O7 晶体进行重结晶操作,进一步分离提纯,故答案为:重结晶;
(6) Na2Cr2O7 溶液具有强氧化性,Na2Cr2O7 溶液与乙醇反应,乙醇可能被氧化为乙醛(CH3CHO)、乙酸(CH3COOH)、甚至可以氧化生成二氧化碳和水,故答案为:乙醛(CH3CHO)、乙酸(CH3COOH)、二氧化碳