题目内容
6.Al单质为面心立方晶体,其晶胞参数(边长)a=0.405nm,晶胞中铝原子的配位数为12.列式表示Al单质的密度$\frac{4×27}{(4.05×1{0}^{-7})^{3}{N}_{A}}$g•cm-3.分析 该晶胞中Al原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,其配位数=3×8×$\frac{1}{2}$,晶胞边长a=0.405nm=4.05×10-7cm,晶胞体积=(4.05×10-7cm)3,密度=$\frac{\frac{M}{{N}_{A}}×4}{V}$.
解答 解:该晶胞中Al原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,其配位数=3×8×$\frac{1}{2}$,晶胞边长a=0.405nm=4.05×10-7cm,晶胞体积=(4.05×10-7cm)3,密度=$\frac{\frac{M}{{N}_{A}}×4}{V}$=$\frac{\frac{27}{{N}_{A}}×4}{(4.05×1{0}^{-7})^{3}}$=$\frac{4×27}{(4.05×1{0}^{-7})^{3}{N}_{A}}$g•cm-3;
故答案为:12;$\frac{4×27}{(4.05×1{0}^{-7})^{3}{N}_{A}}$.
点评 本题考查晶胞计算,为高频考点,侧重考查计算能力及空间想象能力,会根据密度公式计算其密度,为学习难点.

练习册系列答案
相关题目
16.下列说法不正确的是( )
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 某物质的结构为 ,与其互为同分异构且完全水解后产物相同的油脂有两种 ,与其互为同分异构且完全水解后产物相同的油脂有两种 | |
| C. | 用溴水即可鉴别四氯化碳、2-己烯和甲苯 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
17. 柴静在《穹顶之下》中介绍到雾霾中含有较大量的一种突变原和致癌物质--苯并[a]芘(Benzo-a-pyrene)(BAP).苯并芘是一种五环多环芳香烃类(结构如图所示),存在于汽车废气(尤其是柴油引擎)、烟草与木材燃烧产生的烟,以及炭烤食物中.关于苯并[a]芘的下列说法中正确的是( )
柴静在《穹顶之下》中介绍到雾霾中含有较大量的一种突变原和致癌物质--苯并[a]芘(Benzo-a-pyrene)(BAP).苯并芘是一种五环多环芳香烃类(结构如图所示),存在于汽车废气(尤其是柴油引擎)、烟草与木材燃烧产生的烟,以及炭烤食物中.关于苯并[a]芘的下列说法中正确的是( )
 柴静在《穹顶之下》中介绍到雾霾中含有较大量的一种突变原和致癌物质--苯并[a]芘(Benzo-a-pyrene)(BAP).苯并芘是一种五环多环芳香烃类(结构如图所示),存在于汽车废气(尤其是柴油引擎)、烟草与木材燃烧产生的烟,以及炭烤食物中.关于苯并[a]芘的下列说法中正确的是( )
柴静在《穹顶之下》中介绍到雾霾中含有较大量的一种突变原和致癌物质--苯并[a]芘(Benzo-a-pyrene)(BAP).苯并芘是一种五环多环芳香烃类(结构如图所示),存在于汽车废气(尤其是柴油引擎)、烟草与木材燃烧产生的烟,以及炭烤食物中.关于苯并[a]芘的下列说法中正确的是( )| A. | BAP导电性优良,因其有共轭双键结构 | |
| B. | 五环多环芳香烃类都是BAP的同分异构体 | |
| C. | BAP有10种一硝基取代物 | |
| D. | BAP的分子式为C20H12 |
1.X、Y、Z、W是元素周期表中前四周期中的常见元素,其相关信息如下表:
(1)Z位于元素周期表第二周期第VA族,W的基态原子核外有4个未成对电子.
(2)Z的气态氢化物比Y的气态氢化物熔点NH3 (填“高”或“低”),原因是NH3分子间形成氢键
(3)X与Y可形成多种化合物,其中以直线型存在的4核分子中σ键与π键之比为3:2,
(4)Z与X组成的一种气态化合物还原性较强,试写出还原CuO且产物对环境无污染的化学方程式:2NH3+3CuO═3Cu+N2+3H2O
(5)可用YX4还原ZOx以消除污染.
YX4(g)+4ZO2(g)=4ZO(g)+YO2(g)+2X2O(g)△H=-574.0KJ?mol
YX4(g)+4ZO(g)=2Z2(g)+YO2(g)+2X2O(g) H=-1160.0KJ/mol
试写出YX4还原ZO2至Z2的热化学方程式:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-867.0KJ?mol.
| 元素 | 相关信息 |
| X | X的单质是密度最小的气体. |
| Y | Y的一种核素常用于考古且其一种同素异形体是较软的物质之一. |
| Z | Z是其气态氢化物的水溶液显碱性的元素. |
| W | W是地壳中含量居于第二位的金属. |
(2)Z的气态氢化物比Y的气态氢化物熔点NH3 (填“高”或“低”),原因是NH3分子间形成氢键
(3)X与Y可形成多种化合物,其中以直线型存在的4核分子中σ键与π键之比为3:2,
(4)Z与X组成的一种气态化合物还原性较强,试写出还原CuO且产物对环境无污染的化学方程式:2NH3+3CuO═3Cu+N2+3H2O
(5)可用YX4还原ZOx以消除污染.
YX4(g)+4ZO2(g)=4ZO(g)+YO2(g)+2X2O(g)△H=-574.0KJ?mol
YX4(g)+4ZO(g)=2Z2(g)+YO2(g)+2X2O(g) H=-1160.0KJ/mol
试写出YX4还原ZO2至Z2的热化学方程式:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-867.0KJ?mol.
11.下列说法正确的是( )
| A. | 酸、碱、盐都是电解质 | |
| B. | H2O与D2O互称同素异形体 | |
| C. | 石油的分馏和裂化均属于化学变化 | |
| D. | 只含共价键的物质,一定是共价化合物 |
18.在人类文明的历程中,改变世界的事物很多,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化碳、聚乙烯、二氧化硅等多种“分子”改变过人类的世界.
(1)铁原子在基态时,价电子(外围电子)排布式为3d64s2.
(2)硝酸钾中NO3-空间构型为平面三角形,写出与NO3-为等电子体的一种非极性分子化学式BF3[SO3(g)、BBr3等].
(3)6-氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有C、N、O、S.

(4)下列说法正确的有a(填字母序号).
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯分子中有5n个σ键
d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b)kJ
(5)OF2与H2O分子结构十分相似,但H2O分子的极性很强,而OF2分子的极性却很小.试从原子的电负性和中心原子上的孤电子对角度解释原因:从电负性上看,氧与氢的电负性大于氧与氟的电负性差值;②OF2中氧原子上有两对孤电子对,抵消了F-O键中共用电子对偏向F而产生的极性
(6)铜元素与氢元素形成的一种红色离子化合物,其晶体结构如图2所示.则该晶体的化学式为CuH,密度为$\frac{6×65}{\frac{3\sqrt{3}}{2}a{b}^{2}×1{0}^{-30}{N}_{A}}$g.cm-3(列式即可,阿佛加特罗定律常数的值用NA表示)
(1)铁原子在基态时,价电子(外围电子)排布式为3d64s2.
(2)硝酸钾中NO3-空间构型为平面三角形,写出与NO3-为等电子体的一种非极性分子化学式BF3[SO3(g)、BBr3等].
(3)6-氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有C、N、O、S.

(4)下列说法正确的有a(填字母序号).
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯分子中有5n个σ键
d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b)kJ
| 化学键 | Si-Si | O═O | Si-O | |
| 键能(kJ•mol-1) | a | b | c | |
(6)铜元素与氢元素形成的一种红色离子化合物,其晶体结构如图2所示.则该晶体的化学式为CuH,密度为$\frac{6×65}{\frac{3\sqrt{3}}{2}a{b}^{2}×1{0}^{-30}{N}_{A}}$g.cm-3(列式即可,阿佛加特罗定律常数的值用NA表示)
15.下列图象表达正确的是( )
| A. | 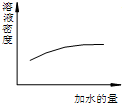 浓硫酸的稀释 浓硫酸的稀释 | |
| B. | 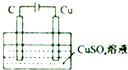 某电极上有铜产生,且溶液中铜离子浓度不变 | |
| C. |  微粒电子数 微粒电子数 | |
| D. | 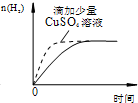 过量的盐酸和等量的锌粉反应 过量的盐酸和等量的锌粉反应 |
10.下列叙述错误的是( )
| A. | 砹化银难溶于水,见光容易分解 | |
| B. | H20、H2S、H2Se随着相对分子质量的增大,沸点逐渐升高 | |
| C. | 因为H2C03比H2Si03酸性强,所以将C02通入N2SiC3溶液中有H2Si03沉淀生成 | |
| D. | 铝和铊同属第IIIA族元素,但氢氧化铊[Tl(OH)3]不一定呈两性 |
 ;
;