题目内容
6.如图为铜-锌-稀硫酸构成的原电池示意图,下列说法正确的是( )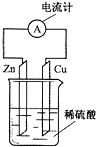
| A. | 锌片为正极,且锌片逐渐溶解 | B. | 铜片为负极,且铜片上有气泡 | ||
| C. | 溶液中的H+移向铜极 | D. | 该装置能将电能转变为化学能 |
分析 铜-锌-稀硫酸构成的原电池中,锌是负极,负极上锌失电子发生氧化反应,铜为正极,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极,结合原电池定义分析解答.
解答 解:A.该原电池中,锌是负极,负极上锌失电子变成锌离子进入溶液导致锌逐渐溶解,故A错误;
B.铜为正极,铜上氢离子得电子生成氢气,所以铜上有气泡生成,故B错误;
C.锌是负极,铜是正极,溶液中的阳离子移向正极,所以H+移向铜极,故C正确;
D.该装置是原电池,是将化学能转变为电能的装置,故D错误;
故选C.
点评 本题考查原电池原理,明确正负极上发生的反应是解本题的关键,难度不大.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
16.下表是元素周期表中短周期元素部分,表中字母分别代表一种元素:
(1)上述化学性质最不活泼的元素是氦(填元素名称).
(2)画出h的原子结构示意图 ,其单质在电子工业上有重要用途,写出工业制取该单质的化学方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
,其单质在电子工业上有重要用途,写出工业制取该单质的化学方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(3)c、d、g离子半径由小到大的顺序是O2->Na+>Al3+ (用离子符号表示).
(4)表中元素g的氢化物稳定性>(填“>”或“<”)元素e的氢化物稳定性.
(5)c元素最高价氧化物的水化物中含有离子键、共价键(填化学键类型),该物质不能储存在带玻璃塞的试剂瓶中的原因:SiO2+2NaOH=Na2SiO3+H2O(用化学方程式表示).
| a | b | ||||||
| e | f | g | |||||
| c | d | h | i | j | |||
(2)画出h的原子结构示意图
 ,其单质在电子工业上有重要用途,写出工业制取该单质的化学方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
,其单质在电子工业上有重要用途,写出工业制取该单质的化学方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.(3)c、d、g离子半径由小到大的顺序是O2->Na+>Al3+ (用离子符号表示).
(4)表中元素g的氢化物稳定性>(填“>”或“<”)元素e的氢化物稳定性.
(5)c元素最高价氧化物的水化物中含有离子键、共价键(填化学键类型),该物质不能储存在带玻璃塞的试剂瓶中的原因:SiO2+2NaOH=Na2SiO3+H2O(用化学方程式表示).
14.将5.6 L(标准状况)乙烯和甲烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了2.8 g.原混合气体中乙烯与甲烷的质量比是( )
| A. | 2:1 | B. | 2:3 | C. | 7:6 | D. | 7:3 |
1.试剂B、C分别是( )
| A. | NaOH、CuSO4 | B. | NaOH、新制Cu(OH)2 | C. | Na2CO3、CuSO4 | D. | H2SO4、新制Cu(OH)2 |
11.下列装置或操作不能达到实验目的是( )
| A. | 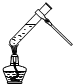 葡萄糖的银镜反应 | B. | 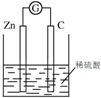 形成原电池 | ||
| C. | 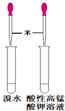 检验苯中有无碳碳双键 | D. | 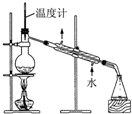 石油的分馏 |
18.下列有关问题,与盐的水解无关的是( )
| A. | 用盐酸除铁锈 | |
| B. | 用纯碱溶液清洗油污 | |
| C. | 加热蒸干AlCl3溶液得到Al(OH)3固体 | |
| D. | 实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 |
15.下列各组顺序的排列不正确的是( )
| A. | 酸性强弱:HClO4>H2SO4>H3PO4 | B. | 离子半径:Na+>Mg2+>Al3+>F- | ||
| C. | 热稳定性:HCl>H2S>PH3>SiH4 | D. | 氧化性:K+<Na+<Mg2+<Al3+ |