��Ŀ����
����Ŀ��ʵ������Ҫʹ��1.0mol/LNaOH��Һ80mL��
(1)���Ƹ�NaOH��Һ��������ƿ�Ĺ����________��
(2)��������ƽ��ȡNaOH����________g��
(3)������ɺ������²�����
A.���ƺõ�NaOH��������ձ��У�����������ˮ�ܽ⡣
B.������ȫ���ܽ����Һ����ת�Ƶ�����ƿ��
C.����������ˮϴ���ձ��Ͳ�����2��3�Σ�ϴ��ҺҲ���ò���������ע������ƿ������ҡ������ƿ��ʹ��Һ��Ͼ��ȡ�
D.����������ƿ������ˮ��Һ��������ƿ���̶�����________cmʱ������_________�μ�����ˮ����Һ�İ�Һ����̶������С�
E.�Ǻ�ƿ�����������µߵ���ҡ�ȡ�
������������ȷ����________(�����)��
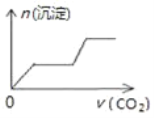
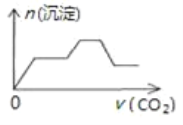
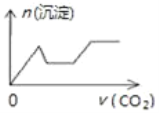
(4)��δ������������C����������ҺŨ��________(�ƫ�ߡ���ƫ�͡�����Ӱ�족����ͬ)��������ʱ����ͼ��������������ҺŨ��________��
(5)ȡ������Һ10mLϡ����50mL������NaOH��Һ�����ʵ���Ũ��Ϊ________��
���𰸡�100mL 4.0 1��2 ��ͷ�ι� B ƫ�� ƫ�� 0.2mol/L
��������
ʵ��������80mL1.0mol/LNaOH��Һ�IJ���Ϊ���ƺõ�NaOH��������ձ��У�����������ˮ�ܽ��������ƹ��壬�ò��������Ͻ��裬��ȴ���ò���������ת�Ƶ�100mL������ƿ�У�Ȼ��ϴ���ձ��Ͳ�����2��3�Σ���ϴҺ�ò���������ת�Ƶ�����ƿ��������ƿ�м�������ˮ����̶���1-2cm�����ý�ͷ�ι���εμ�����ˮ����Һ����̶������У���������ҡ��װƿ��
(1)ʵ������80mL����ƿ������80mL1.0mol/LNaOH��ҺӦѡ��100mL������ƿ���ʴ�Ϊ��100mL��
(2)����n=CV��֪������100mL1.0mol/LNaOH��Һ��Ҫ��NaOH�����ʵ���n=0.1L��1.0mol/L=0.1mol�����������Ƶ�����m=nM=0.1mol��40g/mol=4.0g���ʴ�Ϊ��4.0��
(3)����ʱ��������ƿ�м�������ˮ����̶���1-2cm�����ý�ͷ�ι���εμ�����ˮ����Һ����̶������У�ע���ܽ�ʱ�����������ƹ���ȫ���ܽ⣬��ȴ���ò���������ת�Ƶ�100mL������ƿ�У���B���ʴ�Ϊ��1-2��B��
(4)��δϴ���ܽ�NaOH���ձ��Ͳ��������ᵼ��������ʧ���������Ƶ����ʵ�����С����ҺŨ��ƫ�ͣ�����ʱ��������ƿ�̶��ߣ��ᵼ����Һ�����ƫ����Һ��Ũ��ƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�ƫ�ͣ�
(5)��ϡ�Ͷ��ɿ�֪��ϡ��ǰ�����ʵ����ʵ������䣬����1.0mol/L��0.01L=c��0.05L�����c=0.2 mol/L���ʴ�Ϊ��0.2 mol/L��

����Ŀ��Ǧ��������Ļ�е�ӹ����ܣ������Ʊ��������������ĺϽ𡣹㷺���ڵ�����졢��е��������ҵ���Լ������Է���������
��1��Ǧ����Ҫ�����ʽ�Ƿ�Ǧ��PbS��������ұ��Ǧ�ķ�Ӧ�������£�
2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) ��H=akJ��mol-1
PbS(s)+2O2(g)=PbSO4(s) ��H=bkJ��mol-1
PbS(s)+2PbO(s)=3Pb(s)+SO2(g) ��H=ckJ��mol-1
�����÷�Ǧ���Ǧ������Ҫ�ɷ�ΪPbSO4��ұ��Ǧ������һ�ֿ�����������������Ȼ�ѧ����ʽΪ____��
��2��ǦҲ���Բ����Ȼ�ԭ��ұ����PbO(s)+CO(g)![]() Pb(s)+CO2(g) ��H=dkJ��mol-1����֪�÷�Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���±���
Pb(s)+CO2(g) ��H=dkJ��mol-1����֪�÷�Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���±���
�¶�/�� | 300 | 727 | 1227 |
K | 106.2 | 631 | 17.4 |
��d____0���������=��
����֪ij�¶���K=10�����ܱ������м���������Pb��һ������CO2ƽ��ʱ�����������CO���������Ϊ____��
��3������Һ��ʽǦ�����Կ��ܵļ�����ǦΪ����ʣ�����ܷ�Ӧ��Pb+PbO2+4H+![]() 2Pb2++2H2O
2Pb2++2H2O
���й��ڸõ�ص�˵����ȷ����____��
a.��ŵ�ʱ����Һ��Pb2+Ũ�ȱ��ֲ���
b.�ŵ�ʱ����Һ��H+��PbO2�����ƶ�
c.�ŵ�ʱ�ĸ�����ӦʽΪ��Pb-2e-=Pb2+
d.���ʱ��������ӦʽΪ��Pb2++4OH--2e-=PbO2+2H2O
��4�������������е�Ǧ��Ⱦ���汻�������ӡ���֪������PbԪ����ˮ�еĸ��ִ�����ʽ���ʵ�������������ҺpH�Ĺ�ϵ��ͼ��ʾ��
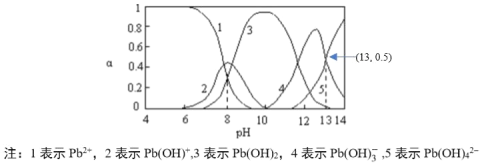
�����Ǧ��Һ����εμ�����������Һ��pH=13ʱ����Ҫ���ӷ�Ӧ����ʽ��_____����ƽ�ⳣ����ֵΪ____��
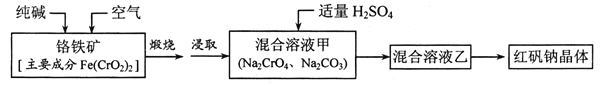
����Ŀ����ˮ���̲��ŷḻ����Դ����ˮ�ۺ����õ�����ͼ���£�

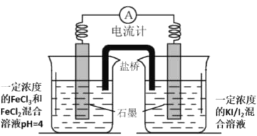
��һ��ij��ѧ�о�С������ͼװ��ģ�ⲽ��I���ʳ��ˮ��������ʯī���缫����

��1��a�缫������_____��������ʯī������缫��ӦʽΪ_________��
��2������������11.2mL����ʱ����״����������Һ��pHΪ______�����Է�Ӧǰ����Һ����ı仯����
������±ˮ���̺��ŷḻ��þ��Դ����MgCl2�ֲ�Ʒ���ᴿ��þ��ұ�����̻ش��������⣺��֪MgCl2�ֲ�Ʒ����Һ�к���Fe2+��Fe3+��Al3+��
�±��������������������pH��
���� | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
��ʼ����pH | 2��7 | 8��1 | 3��8 | 9��5 |
��ȫ����pH | 3��7 | 9��6 | 4��8 | 11��0 |
��3����MgCl2�ֲ�Ʒ����Һ�е�Fe2+ת��ΪFe3+����ѡ�õ�������_____������ţ���ͬ��������_____������Һ��pH����ַ�Ӧ����ˣ��ɵ�MgCl2��Һ��
a��KMnO4 b��H2O2 c��MgO d��NaOH
��4���������MgCl2��H2O���MgCl2�IJ����ǣ�_________��
��������ȡ��ҵ�壺
��5����������ѻ��Br2����������ֽ�Br2��ԭΪBr������Ŀ����_______��
��6��д���������SO2ˮ��Һ����Br2�����ӷ���ʽ��________��