题目内容
【题目】某化学兴趣小组为探究铜跟浓硫酸反应,用下图装置进行有关实验。请回答下列问题:
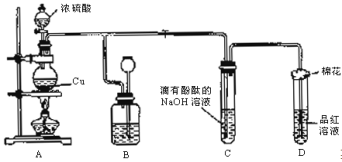
(1)装置A中发生的化学反应的化学方程式为 ;
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是 (填序号);
①水 ②酸性KMnO4 ③Na2CO3溶液 ④饱和的NaHSO3溶液
(3)装置C和D中产生的现象相同,但原因却不同。C中是由于SO2 ,而D中则是由于SO2具有 ;
(4)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是 ;
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色,为了证明蓝色只与Cu2+有关,而与其它离子无关,某同学设计了下列实验,其中对实验目的没有意义的是 (填序号);
①观察稀H2SO4溶液呈无色
②观察CuSO4粉末呈白色
③稀释CuSO4溶液,溶液蓝色变浅
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍显蓝色
(6)若实验中用7.2g铜片和12.5mL18.0ml·L-1的浓硫酸在加热条件充分反应,最终铜片仍有剩余。根据所学的知识,某同学认为溶液中一定还有硫酸剩余,其理由是 。
假定反应前后溶液的体积不变,设剩余硫酸的浓度为amol/L,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾 mol(用含a的代数式表示,要化简)。
【答案】(1)Cu+2H2SO4![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(2)④(3)中和了溶液中的NaOH 漂白性
(4)吸收多余的SO2,防止污染环境(5)②③
(6)反应过程中浓H2SO4被不断消耗,同时生成的水逐渐增多,使浓硫酸逐渐变稀,至一定浓度就不再与铜片反应 a/160
【解析】
试题分析:(1)浓硫酸具有强氧化性,在加热条件下能与铜发生氧化还原反应生成硫酸铜、二氧化硫和水,反应的化学方程式为Cu+2H2SO4![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
(2)SO2易溶于水,具有酸性和还原性,可与酸性KMnO4、Na2SO3溶液反应,难溶于水饱和的NaHSO3溶液,可用排饱和NaHSO3溶液收集,答案选④。
(3)SO2溶液具有酸性,可与NaOH溶液反应,发生SO2+2OH-=SO32-+H2O,滴加酚酞的氢氧化钠溶液褪色,SO2具有漂白性,可使品红溶液褪色,所以装置C和D中产生的现象相同,但原因却不同。C中是由于SO2中和了溶液中的NaOH,而D中则是由于SO2具有漂白性。
(4)二氧化硫有毒,不能排放到空气中,能与氢氧化钠溶液反应,则棉花上可浸有氢氧化钠溶液,吸收多余的SO2,防止污染环境。
(5)①观察稀硫酸溶液呈无色,可说明SO42-无色;②观察CuSO4粉末呈白色,不能证明蓝色只与Cu2+有关;③稀释CuSO4溶液,溶液蓝色变浅,因阳离子和阴离子浓度都变浅,不能证明;④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色,铜离子浓度减小,可说明与铜离子有关;⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色,铜离子物质的量不变,可说明与铜离子有关,则对实验目的没有意义的是②③。
(6)浓硫酸具有强氧化性,而稀硫酸与铜不反应,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,则反应后溶液中一定含有硫酸。剩余硫酸的浓度为amol/L,物质的量为0.0125L×amol/L= 0.0125a mol,氢离子的物质的量为0.025amol,向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,发生反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,则反应消耗硝酸钾a/160mol。