题目内容
【题目】孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:

请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为______(填代号),检验溶液A中Fe3+的最佳试剂为____(填代号)。
a.KMnO4 b.(NH4) 2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、__________、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是______。
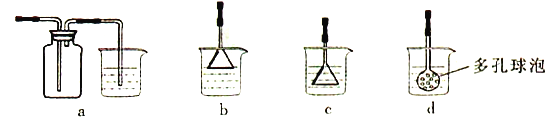
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)___________(填化学式),若实验过程中有氨气逸出,应选用下列______装置回收(填代号)。
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应____,直到_____,用KMnO4标准溶液滴定时应选用____滴定管(填“酸式”或“碱式”)。
【答案】(1) c (2分) d (2分) (2)冷却结晶 (2分) 引流 (2分)
(3)NH3·H2O (2分) b (2分)
(4 平视凹液面(或平视刻度线)(1分) 凹液面的最低点与刻度线相切 (1分) 酸式 (1分)
【解析】试题分析:(1)要制取硫酸铜晶体,就必须除去溶液中的杂质离子,可用沉淀法除去铁离子。因此首先要把溶液中的亚铁离子氧化生成铁离子,但同时又不能引入新的杂质,双氧水的还原产物是水,不会引入杂质。所以答案选C。检验溶液A中Fe3+的最佳试剂是KSCN溶液。(2)要获得CuSO4·5H2O,需要通过加热蒸发、冷却结晶,然后过滤即可。过滤时除烧杯、漏斗外,还需要玻璃棒引流。(3)用于CO2的溶解度很小,所以首先通入氨气,时溶液显碱性,然后再通入CO2即得到碳酸钙固体。用于氨气极易溶于水,所以吸收需要氨气防止倒吸,因此答案选b。(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应平视凹液面(或平视刻度线),直到凹液面的最低点与刻度线相切 ,由于KMnO4溶液有强氧化性能腐蚀橡胶管,滴定时应选用酸式滴定管。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案