题目内容
如图所示,通电一段时间后,Cu电极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为100 mL,则通电前A池中原混合溶液Cu2+的浓度为
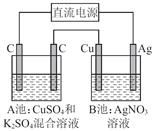
| A.0.05 mol/L | B.0.035 mol/L | C.0.025 mol/L | D.0.020 mol/L |
A
“Cu电极增重2.16 g”那么Cu作阴极,则A池中左电极是阴极,右电极是阳极;结合,Ag++e-=Ag,电极增重2.16 g(即
 ),转移电子0.02 mol。A池中,阳极反应为4OH--4e-=2H2O+O 2↑,转移0.02 mol电子,即得n(O2)=0.005 mol,累计收集气体224 mL(即
),转移电子0.02 mol。A池中,阳极反应为4OH--4e-=2H2O+O 2↑,转移0.02 mol电子,即得n(O2)=0.005 mol,累计收集气体224 mL(即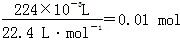 ),那么在阴极还产生0.005 mol H2,阴极反应为2H++2e-=H2↑,转移电子0.01 mol,因此Cu2+放电0.01 mol,Cu2++2e-=Cu,n(Cu2+)=0.005 mol,
),那么在阴极还产生0.005 mol H2,阴极反应为2H++2e-=H2↑,转移电子0.01 mol,因此Cu2+放电0.01 mol,Cu2++2e-=Cu,n(Cu2+)=0.005 mol,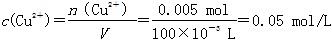 。
。
练习册系列答案
相关题目
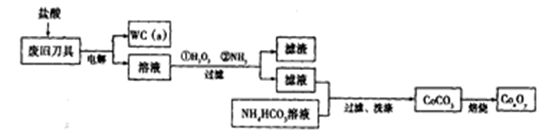
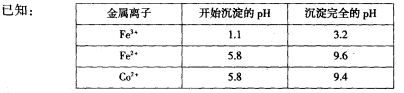
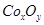 ,并测定其化学式。
,并测定其化学式。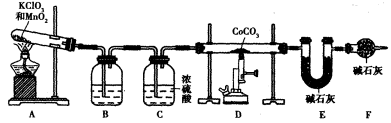
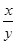 的值______(填“偏大”、“偏小”或“无影响”)。
的值______(填“偏大”、“偏小”或“无影响”)。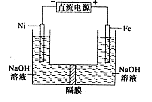
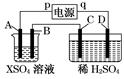
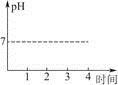
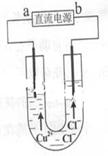

 R2Cu(有机相)+2H+(水相)
R2Cu(有机相)+2H+(水相)