题目内容
【题目】(1)物质的分离与提纯是化学的重点,请根据下列实验目的,分别选择相应的操作和实验装置。下列为操作:
a.蒸馏 b.结晶法 c.加适量水,过滤 d.加热(或灼烧) e.加适量盐酸,蒸发 f.萃取分液 g.分液 h.升华
下列为实验装置:
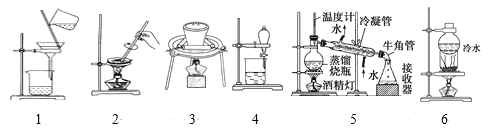
(1)从碘水中提取碘:___、__。(分别填操作序号及实验装置图编号,下同)。
(2)除去氧化钙中的碳酸钙:___、___。
(3)除去硫酸钡中的硝酸钾:___、___。
(4)分离固体细沙和碘的方法:___、___。
(5)除去氯化钠晶体中的碳酸钠:___、__。
(6)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合液(两者互溶):__、_。
【答案】f 4 d 3 c 1 h 6 e 2 a 5
【解析】
(1)从碘水中提取碘:碘在四氯化碳、苯等有机溶剂中的溶解度远大于碘在水中的溶解度,从碘水中提取碘选用萃取分液法,选f分离,为装置4,故答案为:f;4;
(2)除去氧化钙中的碳酸钙:碳酸钙加热分解生成CaO,选d分离,为装置3,故答案为:d;3;
(3)除去硫酸钡中的硝酸钾:硫酸钡不溶于水,硝酸钾溶于水,加适量水后过滤,选c分离,为装置1,故答案为:c;1;
(4)分离固体细沙和碘的方法:加热碘易升华,固体细沙不变,选h分离,为装置6,故答案为:h;6。
(5)除去氯化钠晶体中的碳酸钠:碳酸钠与盐酸反应生成NaCl,NaCl为可溶性固体,用蒸发结晶从NaCl溶液中获得氯化钠晶体,选e分离,为装置2,故答案为:e;2;
(6)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合液(两者互溶):二者互溶,但沸点不同,用蒸馏法分离,选a分离,为装置5,故答案为:a;5。

 阅读快车系列答案
阅读快车系列答案【题目】I.化合物X含有三种元素,其中两种为非金属元素,且原子个数比为1:1,X不溶于水,能溶于强酸。某研究小组为探究其组成和性质,设计并完成了如下实验。
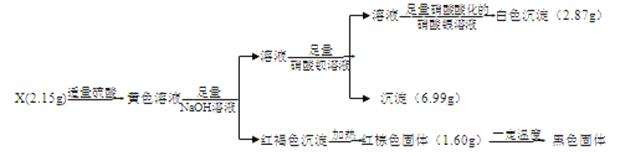
(1)X的化学式是____________________。
(2)写出检验黄色溶液中金属阳离子的实验操作:__________。
(3)黄色溶液中加入铜片,铜片表面被腐蚀,则对应的离子方程式是:_____________________。
II.已知黑色固体中不含单质。为进一步探究其组成,研究小组将上述所得固体全部溶于稀盐酸,配成100mL溶液,每次取20.00mL待测液于锥形瓶中,用2.000×10-2molL-1 KMnO4标准溶液进行滴定,并记录实验的结果如下表:
组次 | 1 | 2 | 3 | 4 |
V标(mL) | 20.00 | 20.02 | 19.99 | 19.99 |
(4)如何判断滴定终点:__________________。
(5)待测液中c(Fe2+) = ____________________。
(6)该黑色固体的化学式用FexOy形式可表示为_______________。