题目内容
【题目】氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(φ)如图所示。
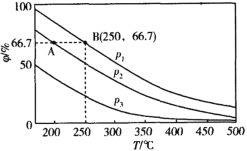
①其中,p1、p2和p3由大到小的顺序是___,其原因是___。
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)___vB(N2)(填“>”“<”或“=”)。
③若在250℃、p1为105Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为___Pa(分压=总压×物质的量分数,保留一位小数)。
【答案】p1>p2>p3 温度相同时,增大压强化学平衡向正反应方向移动,故平衡混合物中氨的体积分数越大压强越大 < 8.3×103
【解析】
①由方程式N2(g)+3H2(g)![]() 2NH3(g)可知,增大压强,平衡正向移动,氨的体积分数越大;
2NH3(g)可知,增大压强,平衡正向移动,氨的体积分数越大;
②温度越大,压强越大,反应速率越大;
③列出三段式,先求出氨的物质的量分数,再代入计算:p(N2)=总压×物质的量分数=105Pa×![]() 。
。
①由N2(g)+3H2(g)![]() 2NH3(g)可知,增大压强,平衡正向移动,由图象可知在相同温度下,平衡后混合物中氨的体积分数(φ)为P1>P2>P3,因此压强关系是P1>P2>P3,故答案为:P1>P2>P3;温度相同时,加压平衡正向移动,故压强越大平衡混合物中氨的体积分数越大;
2NH3(g)可知,增大压强,平衡正向移动,由图象可知在相同温度下,平衡后混合物中氨的体积分数(φ)为P1>P2>P3,因此压强关系是P1>P2>P3,故答案为:P1>P2>P3;温度相同时,加压平衡正向移动,故压强越大平衡混合物中氨的体积分数越大;
②温度越大,压强越大,反应速率越大,p1>p2,由图可知,B对应的温度、压强大,则反应速率大,故答案为:<;
③列出反的三段式:

![]() =0.667,x=0.08
=0.667,x=0.08
p(N2)=总压×物质的量分数=105Pa×![]() =8.3×103;
=8.3×103;
故答案为:8.3×103。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】初始温度为t ℃,向三个密闭的容器中按不同方式投入反应物,发生如下反应:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1,测得反应的相关数据如下:
2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1,测得反应的相关数据如下:
容器 | 容器类型 | 初始体积 | 初始压强/Pa | 反应物投入量/mol | 平衡时Cl2的物质的量/mol | |||
HCl | O2 | Cl2 | H2O | |||||
I | 恒温恒容 | 1L |
| 4 | 1 | 0 | 0 | 1 |
II | 绝热恒容 | 1L | p2 | 0 | 0 | 2 | 2 | a |
III | 恒温恒压 | 2L | p3 | 8 | 2 | 0 | 0 | b |
下列说法正确的是( )
A.反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1
2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1
B.a>1, b>2
C.p2=1.6×105Pa,p3=4×105Pa
D.若起始向容器Ⅰ中充入0.5 mol HCl、0.5 mol O2、0.5 mol Cl2和0.5 mol H2O,则反应向逆反应方向进行
【题目】羰基硫(COS)可用作粮食熏蒸剂,可由CO和H2S在一定条件下反应制得。在2L的密闭容器中发生反应CO(g)+H2S(g)![]() COS(g)+H2(g),有关数据如表所示:
COS(g)+H2(g),有关数据如表所示:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(CO) | n(H2S) | n(CO) | ||
① | 150 | 10 | 10 | 7 |
② | 400 | 20 | 20 | 16 |
下列说法正确的是( )
A.②中CO的平衡转化率为80%
B.400℃时该反应的平衡常数K=![]()
C.该反应是吸热反应
D.①中反应10min达到平衡,0~10min的平均反应速率:v(CO)=0.3mol/(Lmin)