题目内容
【题目】从环己烷可制备1,4-环己二醇,合成步骤如下。试回答:

![]()
![]()
(1)反应①反应类型属于____。
(2)羟基的电子式____。
(3)化合物的结构简式:B____,C_____。
(4)完成以下步骤方程式(注明反应条件)④____。
(5)反应⑤中可能产生一定量的副产物,任写一个其可能的结构简式为___。
(6)反应⑥所用试剂和条件是___。
【答案】取代反应 ![]()
![]()
![]()
 +2NaOH
+2NaOH![]() 2NaCl+2H2O+
2NaCl+2H2O+![]()
 或
或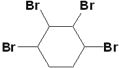 NaOH的水溶液,加热
NaOH的水溶液,加热
【解析】
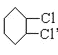
环己烷和氯气发生取代反应生成![]() ,
,![]() 在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为:
在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为:![]() ,A和氯气反应生成B,B发生消去反应生成
,A和氯气反应生成B,B发生消去反应生成![]() ,所以B的结构简式为
,所以B的结构简式为![]() ,则A和氯气发生加成反应生成B,
,则A和氯气发生加成反应生成B,![]() 和溴发生1,4-加成反应生成
和溴发生1,4-加成反应生成![]() ,
,![]() 在氢氧化钠的水溶液、加热条件下发生取代反应生成C为
在氢氧化钠的水溶液、加热条件下发生取代反应生成C为![]() ,
,![]() 和氢气发生加成反应生成
和氢气发生加成反应生成![]() ,据此答题。
,据此答题。
(1)根据上面的分析可知,反应①属于取代反应,故答案为:取代反应;
(2)羟基的电子式为![]() ;故答案为:
;故答案为:![]() ;
;
(3)根据上面的分析可知,B为![]() ,C为
,C为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
(4)④的化学方程式为: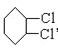 +2NaOH
+2NaOH![]() 2NaCl+2H2O+
2NaCl+2H2O+![]() ,故答案为:
,故答案为: +2NaOH
+2NaOH![]() 2NaCl+2H2O+
2NaCl+2H2O+![]() ;
;
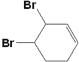
(5)反应⑤为![]() 和溴水发生1,4加成生成
和溴水发生1,4加成生成![]() ,可能生成的副产物为:
,可能生成的副产物为: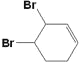 或
或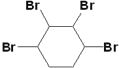 ,故答案为:
,故答案为: 或
或 ;
;
(6)反应⑥为![]() 在氢氧化钠的水溶液、加热条件下发生取代反应生成C为
在氢氧化钠的水溶液、加热条件下发生取代反应生成C为![]() ,所用试剂和条件是,故答案为:氢氧化钠的水溶液、加热。
,所用试剂和条件是,故答案为:氢氧化钠的水溶液、加热。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】用下列试剂和试管中的物质不能完成相应实验目的的是
实验目的 | 试剂 | 试管中的物质 |
| |
A | 鉴别碳酸钠和碳酸氢钠固体 | 稀盐酸 | ①碳酸钠②碳酸氢钠 | |
B | 比较 | 氯水 | ① | |
C | 证明苯分子中没有碳碳双键 |
| ①苯②己烯 | |
D | 探究接触面积对反应速率的影响 | VmL、 | ①ag大理石块②ag大理石粉 |
A.AB.BC.CD.D