题目内容
11.恒容密闭容器中进行的可逆反应2NO2(g)?2NO(g)+O2(g),不能说明该反应达到平衡状态的是( )| A. | 单位时间内生成n mo1 O2的同时生成2n mol NO2 | |
| B. | 混合气体的颜色不再改变 | |
| C. | 混合气体的压强不再改变的状态 | |
| D. | 混合气体的密度不再改变的状态 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、单位时间内生成n mol O2的同时生成2n mol NO2,生成nmol氧气,会消耗2nmol二氧化氮,说明了正逆反应速率相等,达到了平衡状态,故A正确;
B、混合气体的颜色不再改变,说明二氧化氮的浓度不再变化,达到了平衡状态,故B正确;
C、混合气体的压强不再改变,说明气体的物质的量不变,达化学平衡状态,故C正确;
D、混合气体的密度不再改变的状态,由于反应两边都是气体,容器的体积不变,所以反应中密度始终不变,即密度不能作为判断化学平衡的依据,故D错误.
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
6.pH=a的某电解质溶液中,插入两支惰性电极,通直流电一段时间后,溶液的pH<a,则该电解质是( )
| A. | NaOH | B. | HCl | C. | H2SO4 | D. | KCl |
3.在标准状况下将1.92g铜粉投入一定量浓HNO3中随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混和气体1.12L,则混和气体中NO的体积为( )
| A. | 112mL | B. | 1008mL | C. | 224mL | D. | 448mL |
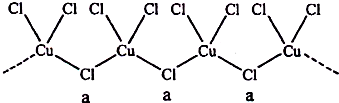
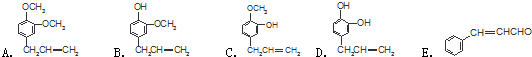
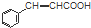 $\stackrel{反应②}{→}$X,
$\stackrel{反应②}{→}$X,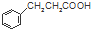 .
. 甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.