题目内容
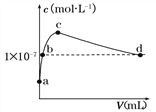
【题目】常温下,向1 L pH=10的 NaOH溶液中持续通入CO2。通入的CO2的体积(V)与溶液中水电离出的OH-离子浓度(c)的关系如图所示。下列叙述不正确的是( )
A. b点溶液中:c(OH-)=1×10-7 mol·L-1
B. a点溶液中:水电离出的c(H+)=1×10-10 mol·L-1
C. c点溶液中:c(Na+)>c(CO![]() )>c(HCO
)>c(HCO![]() )
)
D. d点溶液中:溶液是NaHCO3和H2CO3的混合液
【答案】A
【解析】试题分析:由图像可知,a点对应的溶液为原pH=10的 NaOH溶液,b点对应的溶液为氢氧化钠和碳酸钠的混合溶液,c点对应的溶液为碳酸钠溶液,d点对应的溶液为碳酸氢钠和碳酸的溶液。A. b点对应的溶液为氢氧化钠和碳酸钠的混合溶液,由图可知,其中水电离出的OH-离子浓度为1×10-7 mol·L-1,所以溶液中c(OH-)>1×10-7 mol·L-1,A不正确;B. a点溶液中pH=10,所以水电离出的c(H+)=1×10-10 mol·L-1,B正确;C. c点溶液是碳酸钠溶液,有部分碳酸根离子发生水解生成碳酸氢根离子,所以c(Na+)>c(CO![]() )>c(HCO
)>c(HCO![]() ),C正确;D. d点溶液是NaHCO3和H2CO3的混合液,D正确。本题选A。
),C正确;D. d点溶液是NaHCO3和H2CO3的混合液,D正确。本题选A。

练习册系列答案
相关题目