题目内容
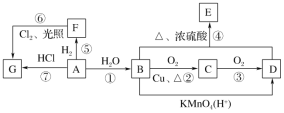
【题目】A、B、C、D四物质有如下转化关系(反应条件和部分产物已略去):A![]() B
B![]() C
C![]() D。回答下列问题:
D。回答下列问题:
(1)若A为气态氢化物和D能通过化合反应生成一种盐,则:
①简述检验A气体的方法_________________________________________;
②写出D制备B的离子方程式_________________________________________;
③写出由A生成B的化学方程式_________________________________________;
④某同学用干燥的圆底烧瓶收集一瓶A气体,用滴入酚酞的水做喷泉实验,能观察到美丽的红色喷泉。用方程式解释喷泉呈红色的原因______________________________;
(2)若A与B反应能生成一种淡黄色固体单质。写出B→C的化学方程式_____________;
(3)若A是金属单质,C是一种淡黄色固体。写出C的电子式________说出C的一种用途_______。
【答案】用湿润的红色石蕊试纸检验,若试纸变蓝,则为氨气 3Cu+8H++2NO3- = 3Cu2++2NO↑+4H2O 4NH3+5O2![]() 4NO+6H2O NH3+ H2ONH3H2ONH4++ OH- 2SO2+O2
4NO+6H2O NH3+ H2ONH3H2ONH4++ OH- 2SO2+O2![]() 2SO3
2SO3 ![]() 做供氧化剂 /漂白剂/氧化剂
做供氧化剂 /漂白剂/氧化剂
【解析】
(1)若A为气态氢化物且和D能通过化合反应生成一种盐,则A为NH3,B为NO,C为NO2,D为HNO3。则:
①NH3与水反应生成NH3·H2O,NH3·H2O显碱性,可使红色石蕊试纸变蓝,所以可用湿润的红色石蕊试纸检验氨气,若试纸变蓝,则为氨气,故答案为:用湿润的红色石蕊试纸检验,若试纸变蓝,则为氨气;
②B为NO、D为HNO3,稀硝酸和Cu反应可产生NO,该反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
③A为NH3、B为NO,由A生成B的化学方程式4NH3+5O2![]() 4NO+6H2O;故答案为:4NH3+5O2
4NO+6H2O;故答案为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
④氨气与水反应生成了一水合氨,一水合氨电离产生了OH-,反应方程式为NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,所以喷泉呈红色,故答案为:NH3+ H2ONH3H2ONH4++ OH- ;
NH4++OH-,所以喷泉呈红色,故答案为:NH3+ H2ONH3H2ONH4++ OH- ;
(2)若A与B反应能生成一种淡黄色固体单质,该单质为S,则A为H2S,B为SO2,C为SO3,D为H2SO4,B→C的化学方程式为: 2SO2+O2![]() 2SO3,故答案为: 2SO2+O2
2SO3,故答案为: 2SO2+O2![]() 2SO3;
2SO3;
(3)若A是金属单质,C是一种淡黄色固体,则A是Na,B是Na2O,C是Na2O2,D是NaOH,Na2O2属于离子化合物,其电子式为![]() ,Na2O2与二氧化碳反应生成氧气,所以Na2O2可做供氧化剂 /漂白剂/氧化剂,故答案为:
,Na2O2与二氧化碳反应生成氧气,所以Na2O2可做供氧化剂 /漂白剂/氧化剂,故答案为:![]() ;做供氧化剂 /漂白剂/氧化剂。
;做供氧化剂 /漂白剂/氧化剂。