题目内容
二甲醚是—种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
请回答下列问题:
(1)煤的气化的主要化学反应方程式为_______________________________________。
(2)煤的气化过程中产生的有害气体用溶液吸收,生成两种酸式盐,该反应的
化学方程式为__________________________________________________________。
(3)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g);△H=-90.8kJ·mol-1
CH3OH(g);△H=-90.8kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g);△H=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g);△H=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g);△H=-41.3kJ·mol-1
CO2(g)+H2(g);△H=-41.3kJ·mol-1
总反应:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的△H= ;
CH3OCH3(g)+CO2(g)的△H= ;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
________________(填字母代号)。
a.高温b.加入催化剂c.减少CO2的浓度d.增加CO的浓度e.分离出二甲醚
(4)已知反应②2CH3OH(g)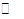 CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。
此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L) | 0.44 | 0.6 | 0.6 |
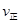 _______
_______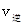 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②若加入CH3OH后,经l0min反应达到平衡,此时c(CH3OH)=__________;该时
间内反应速率v(CH3OH)=__________________。
H2(2分)
(2)H2S+Na2CO3=NaHS+NaHCO3(2分)
(3)-246.4kJ·mol―1(2分) C、e(2分)
(3)①>(2分)②0.04mol /L(2分)0.16mol· L―1· In―1(2分)
解析试题分析:(1)碳和水反应生成一氧化碳和氢气的化学方程式为:C+H2O CO+H2,故答案为:C+H2O
CO+H2,故答案为:C+H2O CO+H2;
CO+H2;
(2)H2S和H2CO3均是二元酸,它们都存在酸式盐NaHS和NaHCO3,二者反应的化学方程式为H2S+Na2CO3=NaHS+NaHCO3,故答案为:H2S+Na2CO3→NaHS+NaHCO3;
(3)由盖斯定律可知,通过①×2+②+③可得所求反应方程式,则△H=-90.8kJ·mol-1×2-23.5kJ·mol-1-41.3kJ·mol-1=-246.4kJ·mol-1,一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,应使平衡向正反应方向移动,可减少CO2的浓度或分离出二甲醚,由于反应放热,升高温度平衡向你反应方向移动,转化率减小,催化剂不影响平衡移动,而增加CO的浓度,CO的转化率反而减小,故答案为:246.4;c;
(4)该反应的平衡常数表达式为:K= ,
,
将所给浓度带入平衡常数表达式: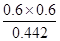 =1.86<400,故反应向正反应方向进行,正反应速率大于逆反应速率;
=1.86<400,故反应向正反应方向进行,正反应速率大于逆反应速率;
2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
某时刻浓度(mol·L-1):0.44 0.6 0.6
转化浓度(mol·L-1):2x x x
平衡浓度(mol·L-1):0.44-2x 0.6+x 0.6+x
K=
,解得x=0.2mol·L-1,
故平衡时c(CH3OH)=0.44mol·L-1-0.2mol·L-1×2=0.04mol·L-1,
起始时在密闭容器中加入CH3OH,
则起始时甲醇的浓度为0.44moL·L-1+0.6mol·L-1×2=1.64mol·L-1,平衡时c(CH3OH)=0.04mol·L-1,
则10min转化甲醇1.64moL·L-1-0.04moL·L-1=1.6mol·L-1,
所以甲醇的反应速率为v(CH3OH)= ="0.16" mol/(L·min),
="0.16" mol/(L·min),
故答案为:>;1.64 mol·L-1;0.16 mol/(L·min)
考点:煤的干馏和综合利用;化学平衡的影响因素;化学平衡的计算

 名校课堂系列答案
名校课堂系列答案化学反应变化过程及结果的研究。按要求回答问题:
(1)关于反应过程中能量变化的研究:
则:2CO(g)+O2(g)=2CO2(g)△H= kJ·mol-1。
(2)关于反应速率和限度的研究:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:
2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l),该反应的平衡常数(K)和温度(T / ℃)关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数(K)和温度(T / ℃)关系如下:
| T / ℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
①焓变ΔH _______0 (填“>”、“<”或“=”)。
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
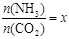 ,下图(1)是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。
,下图(1)是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。
③上图中的B点处,NH3的平衡转化率为 。
(3)关于电化学的研究:
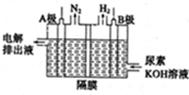
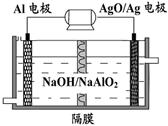
铝是日常生活中用途最多的金属元素,下图为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝电极反应式为 。用该电池电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如下图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为 。

(4)关于电离平衡的研究:
人体血液里存在重要的酸碱平衡:
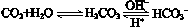 ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:| c(HCO3-)∶c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
试回答:
正常人体血液中,HCO3-的水解程度 电离程度(填“大于”、“小于”、“等于”);
②人体血液酸中毒时,可注射缓解 (填选项);
A.NaOH溶液 B.NaHCO3溶液 C.NaCl溶液 D.Na2SO4溶液
③ pH=7.00的血液中,c(H2CO3) c(HCO3-) (填“<”、“>”、“=”)

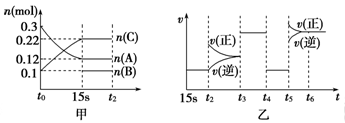
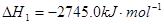


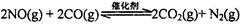 。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断: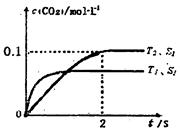
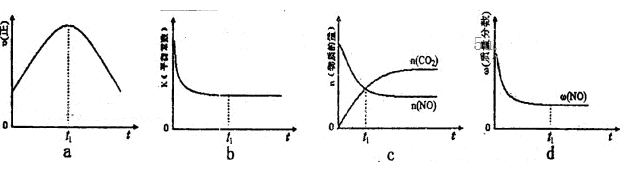
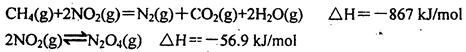
 CO(g)+3H2(g),试回答下列问题。
CO(g)+3H2(g),试回答下列问题。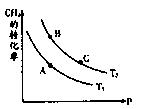

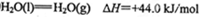
 MnO4-+
MnO4-+