题目内容
【题目】根据信息填空
①某元素原子基态核外电子有 14 种不同的运动状态,该元素位于第_____周期第_____族
②外围电子排布式为 3d54s2 的原子,其原子结构示意图为_____,其最高正价为_____价
③Fe2+的价电子排布图为_____
④33 号元素的核外电子排布式简写形式为_____,属于__________区
⑤前四周期未成对电子最多的元素,其基态核外电子占据的轨道数目为_____
⑥《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3 中,阴离子空间构型为_____,C 原子的杂化形式为___________。
【答案】三 Ⅳ![]()
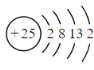 +7
+7 
![]()
![]() 15 三角形
15 三角形 ![]()
【解析】
(1)原子核外有多少个电子,就有多少种运动状态不同的电子,某元素原子基态核外电子有 14 种不同的运动状态,则该元素的原子序数位 14,为 ![]() 元素,位于第三周期Ⅳ
元素,位于第三周期Ⅳ![]() 族。
族。
故答案为:三;Ⅳ![]() 。
。
(2)外围电子排布式为 ![]() 的原子为
的原子为 ![]() 原子,原子序数为 25,其原子结构示意图为
原子,原子序数为 25,其原子结构示意图为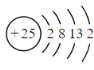
![]() ,
,![]() 原子最多可失去 7个电子,其最高正化合价为 +7 价。
原子最多可失去 7个电子,其最高正化合价为 +7 价。
故答案为: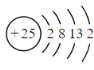
![]() ;+7。
;+7。
(3)![]() 原子的价电子排布式为
原子的价电子排布式为 ![]() ,失去
,失去 ![]() 个电子形成
个电子形成 ![]() ,
,![]() 的价电子排布式为
的价电子排布式为 ![]() ,价电子排布图为
,价电子排布图为
![]() 。
。
故答案为: 。
。
(4)33 号元素为 ![]() 元素,其核外电子排布式简写形式为
元素,其核外电子排布式简写形式为 ![]() ,属于
,属于 ![]() 区。
区。
故答案为:![]() ;
;![]() 。
。
(5)前四周期未成对电子最多的元素为 ![]() 元素,其基态原子核外电子排布式为
元素,其基态原子核外电子排布式为 ![]() ,由于
,由于 ![]() 能级有
能级有 ![]() 个轨道,
个轨道,![]() 能级有
能级有 ![]() 个轨道,
个轨道,![]() 能级有
能级有 ![]() 个轨道,所以
个轨道,所以 ![]() 原子电子占据的轨道数目为:
原子电子占据的轨道数目为:![]() 。
。
故答案为:15。
(6)ZnCO3中阴离子为![]() ,
,![]() 原子所连接的σ键数为
原子所连接的σ键数为![]() ,孤电子对数
,孤电子对数![]() ,所以
,所以![]() 原子的杂化形式为
原子的杂化形式为 ![]() ,
,![]() 的空间构型为三角形。
的空间构型为三角形。
故答案为:三角形;![]() 。
。

 阅读快车系列答案
阅读快车系列答案