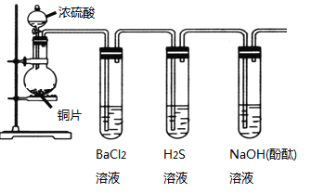
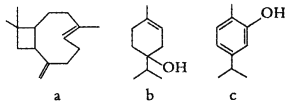
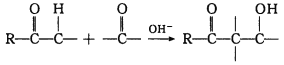
题目内容
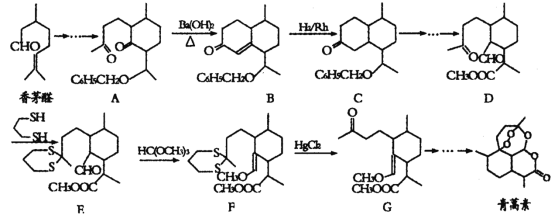
【题目】α—甲基苯乙烯(AMS)在有机合成中用途广泛,以下是用苯为原料合成AMS,并进一步制备香料龙葵醛的路线:
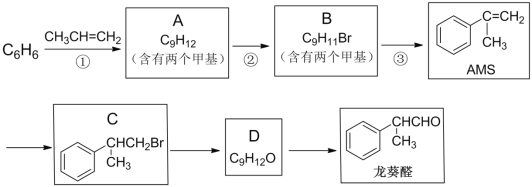
完成下列填空:
(1)反应①的反应类型是____;反应③所需的试剂与条件是____。
(2)写出反应②的化学方程式:____。
(3)AMS可以自身聚合,写出该高聚物的结构简式:____。
(4)写出同时满足下列条件的龙葵醛的一种同分异构体的结构简式:____。
i. 苯环上的一氯代物有两种
ii. 分子中没有甲基
iii. 能与金属钠产生H2
(5)有人认为仅用反应②就能得到C,事实证明产物中C的含量远远小于B。由该事实可以得到的结论是____。
(6)设计一条由AMS合成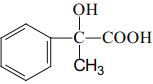 的合成路线____。(合成路线常用的表示方式为:A
的合成路线____。(合成路线常用的表示方式为:A ![]() B。。。
B。。。![]() 目标产物)
目标产物)
【答案】加成反应 NaOH醇溶液、加热 ![]() +Br2
+Br2![]()
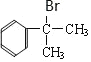 +HBr
+HBr 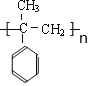
![]() 或
或![]() 或
或![]() 中的任意一种 与苯环直接相连碳上氢更容易被取代(
中的任意一种 与苯环直接相连碳上氢更容易被取代(![]() 氢原子比—CH3氢原子更易被取代)
氢原子比—CH3氢原子更易被取代) ![]()
![]()
【解析】
用苯为原料合成AMS,由合成流程可知反应①为苯与丙烯的加成反应生成![]() ,则A为
,则A为![]() ,在光照条件下发生侧链上取代反应生成B(含两个甲基),则B为
,在光照条件下发生侧链上取代反应生成B(含两个甲基),则B为 ;B发生消去反应生成AMS为
;B发生消去反应生成AMS为![]() ;AMS再与溴化氢发生加成反应生成
;AMS再与溴化氢发生加成反应生成![]() ,
,![]() 在碱性条件下加热,发生水解反应生成B为
在碱性条件下加热,发生水解反应生成B为![]() ,B发生催化氧化反应生成龙葵醛;
,B发生催化氧化反应生成龙葵醛;
(6)由AMS合成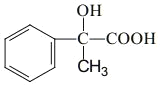 ,先与氯气发生加成反应,再水解,最后发生氧化反应。
,先与氯气发生加成反应,再水解,最后发生氧化反应。
(1)反应①为苯与丙烯的加成反应,其反应类型是加成反应;反应③为 的消去反应,反应所需的试剂与条件是NaOH醇溶液、加热,
的消去反应,反应所需的试剂与条件是NaOH醇溶液、加热,
故答案为:加成反应;NaOH醇溶液、加热;
(2)反应②为苯丙烷与溴单质发生取代反应的过程,其化学方程式为![]() +Br2
+Br2![]()
 +HBr;
+HBr;
(3)AMS可以自身聚合,该高聚物的结构简式为 ;
;
(4)龙葵醛的一同分异构体满足苯环上的一溴代物有两种,则说明苯环上有两个取代基,属于对位关系;能与金属钠产生H2,则说明分子中含有羟基又满足没有甲基的条件,则该分子的结构简式为![]() 或
或![]() 或
或![]() ,
,
故答案为:![]() 或
或![]() 或
或![]() 中的任意一种;
中的任意一种;
(5)取代反应副产物较多,而且取代反应与分子结构有关,若A直接用过取代反应
得到C,则含量远远小于B,因与苯环直接相连碳上氢更容易被取代(![]() 氢原子比—CH3氢原子更易被取代),故答案为:与苯环直接相连碳上氢更容易被取代(
氢原子比—CH3氢原子更易被取代),故答案为:与苯环直接相连碳上氢更容易被取代(![]() 氢原子比—CH3氢原子更易被取代);
氢原子比—CH3氢原子更易被取代);
6)根据上述合成路线可知,由AMS合成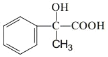 ,先与溴发生加成反应,再水解,最后发生氧化反应,合成流程为:
,先与溴发生加成反应,再水解,最后发生氧化反应,合成流程为:![]()
![]() 。
。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案【题目】下面是某科研小组利用废铁屑还原浸出软锰矿(主要成分为MnO2)制备硫酸锰及电解其溶液制锰的工艺流程图:
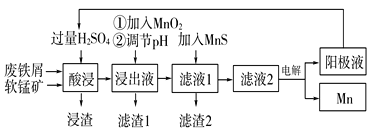
已知:①浸出液中主要含有Fe3+、Fe2+、Co2+、Ni2+等杂质金属离子;
②生成氢氧化物的pH见下表:
物质 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
开始沉淀的pH | 7.5 | 2.7 | 7.7 | 7.6 | 8.3 |
完全沉淀的pH | 9.7 | 3.7 | 8.4 | 8.2 | 9.8 |
请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是____。
(2)流程图中“①加入MnO2”的作用____,MnO2还可以用其他试剂____(填化学式)代替。
(3)流程图中“②调节pH”可以除去某种金属离子,应将溶液pH调节控制的范围是___~7.6。上述流程中,能循环使用的一种物质是___(填化学式)。
(4)向滤液Ⅰ中加入MnS的作用是除去Co2+、Ni2+等离子,其中可以发生反应为MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)等。当该反应完全后,滤液2中的Mn2+与Ni2+的物质的量浓度之比是___[已知Ksp(MnS)=2.8×10-10,Ksp(NiS)=2.0×10-21]。
(5)在适当条件下,在MnSO4、H2SO4和H2O为体系的电解液中电解也可获得MnO2,其阳极电极反应式为____。
(6)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___。
时,z=___。