题目内容
【题目】席夫碱类化合物在催化、药物等方面用途广泛。某种席夫碱的合成路线①如下:
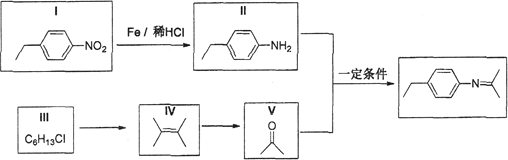
(1)Ⅰ的分子式为__________,1molV完全燃烧至少需要消耗__________mol O2;
(2)III与NaOH水溶液共热反应,化学方程式为___________________________;
(3)IV发生聚合反应生成的高分子化合物的结构简式为_____________________;
(4)结合合成路线①,分析以下合成路线②:
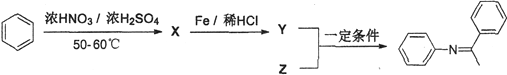
X的结构简式为__________,Z的结构简式为__________。
【答案】C8H9NO2 4 CH3CH(CH3)CCl(CH3)2+NaOH![]() CH3CH(CH3)COH(CH3)2+NaCl
CH3CH(CH3)COH(CH3)2+NaCl 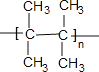
![]()
![]()
【解析】
(1)Ⅰ的结构简式为![]() ,则其分子式为:C8H9NO2;Ⅴ的分子式为C3H6O,其完全燃烧生成二氧化碳和水的化学方程式为C3H6O+4O2
,则其分子式为:C8H9NO2;Ⅴ的分子式为C3H6O,其完全燃烧生成二氧化碳和水的化学方程式为C3H6O+4O2![]() 3CO2+3H2O,则1molV完全燃烧消耗4molO2,故答案为C8H9NO2;4;
3CO2+3H2O,则1molV完全燃烧消耗4molO2,故答案为C8H9NO2;4;
(2)Ⅲ的分子式为C6H13Cl,属于饱和一氯代烃,在NaOH醇溶液中发生消去反应生成IV,根据IV的结构简式知III的结构简式为CH3CH(CH3)CCl(CH3)2,III在NaOH的水溶液中水解生成醇,反应方程式为:CH3CH(CH3)CCl(CH3)2+NaOH![]() CH3CH(CH3)COH(CH3)2+NaCl,故答案为CH3CH(CH3)CCl(CH3)2+NaOH
CH3CH(CH3)COH(CH3)2+NaCl,故答案为CH3CH(CH3)CCl(CH3)2+NaOH![]() CH3CH(CH3)COH(CH3)2+NaCl;
CH3CH(CH3)COH(CH3)2+NaCl;
(3)Ⅳ的结构简式为(CH3)2C=C(CH3)2,结构中含碳碳双键,发生加聚反应生成的高分子化合物为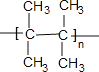 ,故答案为
,故答案为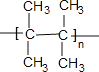 ;
;
(4)苯与浓硝酸、浓硫酸共热到50~60℃发生硝化反应生成硝基苯和水,则X的结构简式为:![]() ,根据I→II可知,X发生还原反应生成Y,Y的结构简式为
,根据I→II可知,X发生还原反应生成Y,Y的结构简式为![]() ,Y与Z反应生成
,Y与Z反应生成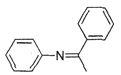 ,仿路线①中II和V的反应知,Z的结构简式为
,仿路线①中II和V的反应知,Z的结构简式为![]() ,故答案为
,故答案为![]() ;
;![]() 。
。
【点晴】
本题考查有机物的推断与合成,注意利用各物质的结构与反应条件进行推断,需要学生熟练掌握官能团的性质与转化,既注重基础知识巩固训练,又较好的考查学生分析推理能力与知识迁移应用。

【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。
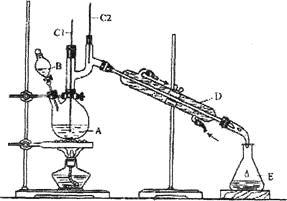
发生的反应如下:
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm﹣3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。回答下列问题:
(1)上述装置图中,B仪器的名称是__________,D仪器的名称是__________;
(2)加入沸石的作用是__________;
(3)分液漏斗使用前必须进行的操作是__________ (填正确答案标号);
a.润湿 b.干燥 c.检漏 d.标定
(4)将正丁醛粗产品置于分液漏斗中分水时,水在__________层(填“上”或“下”);
(5)反应温度应保持在90~95℃。其原因是______________________________;
(6)本实验中,正丁醛的产率为__________%。
【题目】 下表为元素周期表中第四周期的部分元素(从左到右按原子序数递增排列),根据要求回答下列问题:
K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(1)以上元素的基态原子的电子排布中,4s轨道上只有1个电子的元素有______(填元素名称)。
(2)以上元素中,属于s区的元素有_____种,属于d区的元素有______种。
(3)第一电离能I1(Cr)________I1(Co)(填“>”、“<”或“=”,下同)。
(4)现有含钛的两种颜色的晶体,Ti3+的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的![]() 。试推断紫色晶体的化学式为_________。
。试推断紫色晶体的化学式为_________。
(5)含有元素K的盐的焰色反应为__________色。许多金属盐都可以发生焰色反应,其原因是____________。
【题目】某学生用0.1000mol·L-1标准NaOH溶液滴定未知浓度的盐酸,其操作为以下几步:
A.用标准NaOH溶液润洗碱式滴定管2~3次
B.取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
C.把盛有标准NaOH溶液的碱式滴定管固定好,挤压玻璃珠,使滴定管尖嘴充满溶液
D.调节液面至“0”或“0”刻度以下,记下读数
E.移取25.00mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定到终点,并记下滴定管液面的读数
(1)下图中属于碱式滴定管的_____(选填:“甲”、“乙”)。

(2)判断到达滴定终点的实验现象是_____。
(3)上述E步操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响是_____(填“偏大”或“偏小”或“无影响”)。
(4)若平行实验三次,记录的数据如下表
滴定次数 | 待测溶液的体积(/mL) | 标准NaOH溶液的体积 | |
滴定前读数(/mL) | 滴定后读数(/mL) | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
试计算待测盐酸的物质的量浓度(写出计算过程)________。