题目内容
20.可逆反应:2SO2+O2$\stackrel{催化剂}{?}$2SO3,已知生成2mol SO3时放出的热量为Q,2mol SO2和1mol O2在相同条件下反应生成SO3放出的热量为Q2,则( )| A. | Q2=Q1 | B. | Q2<Q1 | C. | Q2>Q1 | D. | Q2≥Q1 |
分析 根据可逆反应的特点可知,可逆反应是不能进行到底的反应,即反应后的体系中含有所有反应物和生成物,反应热与化学计量数成正比.
解答 解:若将2mol SO2和1molO2在相同条件下放入密闭容器发生反应,因2SO2+O2?2SO3是可逆反应,则2molSO2和1mol O2不会完全反应生成2molSO3,即生成SO3的量小于2mol,根据反应2SO2+O2?2SO3,当生成2molSO3时放出热量为Q,则生成小于2mol的 SO3 时放出的热量必小于Q,即Q2<Q,
故选B.
点评 本题考查可逆反应与反应热间的关系,掌握可逆反应的特点是解答该题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.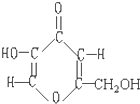 曲酸是一种非常有潜力的食品添加剂.经测定曲酸的分子式为C6H6O4,结构式如图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为( )
曲酸是一种非常有潜力的食品添加剂.经测定曲酸的分子式为C6H6O4,结构式如图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为( )
 曲酸是一种非常有潜力的食品添加剂.经测定曲酸的分子式为C6H6O4,结构式如图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为( )
曲酸是一种非常有潜力的食品添加剂.经测定曲酸的分子式为C6H6O4,结构式如图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为( )| A. | 能发生酯化反应 | B. | 易溶于水、醇 | C. | 具有抗氧化性 | D. | 具有强酸性 |
11.下述实验可以达到预期目的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 将少两KCl晶体加人到如下反应体系中:FeCl3+3KSN?Fe(SCN)3+3KC1 | 证明浓度的改变可导致平衡移动 |
| B | 向某品牌的食盐水中加人几滴淀粉试液 | 确定该品牌食盐是否为加碘盐 |
| C | 将KMnO4溶液加人到丙烯醇(CH2=CHCH2OH)中 | 验证KMnO4能氧化一OH |
| D | 在两支试管中各加人2mL5%H2O2溶液,洱分別滴人0.1mol/L.FeCl3 和CuSO4溶液液各 1ml. | 研究不同催化剂对H2O2分解速率的催化效率 |
| A. | A | B. | B | C. | C | D. | D |
15.下列说法正确的是( )
| A. | 杂化轨道不可以参与π键的形成 | B. | 多原子单质分子都是非极性分子 | ||
| C. | 共价键都有方向性 | D. | 共价化合物中可以含有离子键 |
5.下列物质属于等电子体一组的是( )
| A. | NH3和NH4+ | B. | H2O和CH4 | C. | CO2、NO2 | D. | B3H6N3和C6H6 |
12.既有离子键又有共价键的化合物是( )
| A. | NaCl | B. | H2O | C. | HCl | D. | NaOH |
9.X、Y、Z、W四种主族元素,若X的阳离子与Y的阴离子具有相同的电子层结构,W的阳离子的氧化能力大于等电荷数的X阳离子的氧化能力,Z、Y两元素的最高氧化物对应的水化物的分子式相似,但后者的酸性较前者强,则这四种元素的原子序数由大到小的排列顺序是( )
| A. | X>W>Z>Y | B. | W>X>Y>Z | C. | Z>X>Y>W | D. | X>Z>Y>W |
10.下列离子方程式正确的是( )
| A. | 向KAl(SO4)2溶液中滴加Ba(OH)2溶液至Al3+恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| B. | 向NH4HSO4溶液中滴加过量NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$H2O+NH3↑ | |
| C. | 向AlCl3溶液中滴加过量氨水:Al3++4NH3?H2O═[Al(OH)4]-+4NH4+ | |
| D. | FeO溶于稀硝酸中:FeO+2H+═Fe2++H2O |